题目内容
18.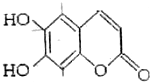 某有机物(结构如图)的一种同分异构体同时满足下列条件:
某有机物(结构如图)的一种同分异构体同时满足下列条件:①苯环上有3个取代基,其中两个是酚羟基;
②能与NaHCO3溶液反应;
③核磁共振氢谱共有4组峰且峰面积之比为1:1:2:2.
写出该同分异构体的结构简式:
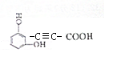 .
.
分析 有机物(结构如图)的分子式为C9 H6O4,其苯环上共有3个取代基(其中两个是酚羟基)、能与碳酸氢钠溶液反应含有羧基,故剩余的C链上部含有H,故另一侧链是丙炔酸基,据此解题.
解答 解:有机物(结构如图)的分子式为C9 H6O4,其苯环上共有3个取代基(其中两个是酚羟基)、能与碳酸氢钠溶液反应含有羧基,故剩余的C链上部含有H,故另一侧链是丙炔酸基,则满足此条件的有机物羟基有邻位、间位和对位,加上另一侧链分别有2种、3种和1种,故总共6种,核磁共振共有4组峰且峰面积之比为1:1:2:2的是: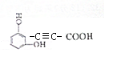 ,故答案为:
,故答案为: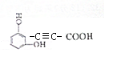 .
.
点评 本题考查有机物的结构,明确有机物中存在的官能团及其性质是解本题关键,注意结合题给信息进行分析,难点是同分异构体种类的判断,题目难度中等.

练习册系列答案
相关题目
11.下列关于有机化合物的说法正确的是( )
| A. | 戊烷有两种同分异构体 | |
| B. | 乙烷,乙醇和苯均不能使酸性高锰酸钾褪色 | |
| C. | 乙醇,乙酸和乙酸乙酯可用碳酸钠溶液加以区别 | |
| D. | 乙烯,聚氯乙烯和苯分子均含有碳碳双键 |
12.实验室从含碘废液(含有H2O、CCl4、I2、I-等)中回收碘,操作过程如下:
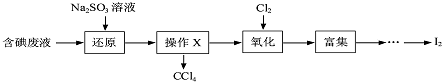
(1)向废液中加入Na2SO3 溶液,发生“还原”反应的离子方程式为SO32-+I2+H2O=2I-+SO42-+2H+.
(2)“氧化”操作在三颈烧瓶中进行(如图一),将溶液用盐酸调至pH约为2,缓慢通入Cl2.实验用水浴控制在40℃左右的较低温度下进行的原因是使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化).
(3)某研究小组用图二装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色.研究小组对所得无色溶液中碘元素的存在形态提出了以下假设:
假设一:没有I2形态;假设二:没有I-形态;假设三:有IO3-形态.
①请设计实验证明假设一成立(试剂自选).
②若假设三成立,请写出生成IO3-的离子方程式I2+5Cl2+6H2O=10Cl-+2IO3-+12H+.
(4)该研究小组还进行了对加碘盐中KIO3含量测定的如下实验:
①准确称取加碘盐m g于烧杯中,加入适量蒸馏水和过量的KI,再滴入适量的稀硫酸,充分反应,将所得混合液配成250.00mL待测溶液.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉试液,用c mol•L-1 Na2S2O3标准液滴定至终点,重复3次,测得平均值为V mL.
已知:IO3-+5I-+6H+=3H2O+3I2,I2+2S2O32-=2I-+S4O62-.测定时,判断达到滴定终点的现象为溶液由蓝色变为无色,且半分钟不变色.由测定数据可求得该样品中含KIO3的质量分数为$\frac{21.4CV}{6m}$%(用含m、c、V的代数式表示,Mr(KIO3)=214 ).
②在滴定操作正确无误的情况下,用此种测定方法测得的结果往往偏高,其原因是受空气的影响,请用离子方程式表示产生这一影响的原因4I-+O2+4H+=2I2+2H2O.


(1)向废液中加入Na2SO3 溶液,发生“还原”反应的离子方程式为SO32-+I2+H2O=2I-+SO42-+2H+.
(2)“氧化”操作在三颈烧瓶中进行(如图一),将溶液用盐酸调至pH约为2,缓慢通入Cl2.实验用水浴控制在40℃左右的较低温度下进行的原因是使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化).
(3)某研究小组用图二装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色.研究小组对所得无色溶液中碘元素的存在形态提出了以下假设:
假设一:没有I2形态;假设二:没有I-形态;假设三:有IO3-形态.
①请设计实验证明假设一成立(试剂自选).
| 实验操作 | 预期现象 | 结论 |
| 假设一成立 |
(4)该研究小组还进行了对加碘盐中KIO3含量测定的如下实验:
①准确称取加碘盐m g于烧杯中,加入适量蒸馏水和过量的KI,再滴入适量的稀硫酸,充分反应,将所得混合液配成250.00mL待测溶液.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉试液,用c mol•L-1 Na2S2O3标准液滴定至终点,重复3次,测得平均值为V mL.
已知:IO3-+5I-+6H+=3H2O+3I2,I2+2S2O32-=2I-+S4O62-.测定时,判断达到滴定终点的现象为溶液由蓝色变为无色,且半分钟不变色.由测定数据可求得该样品中含KIO3的质量分数为$\frac{21.4CV}{6m}$%(用含m、c、V的代数式表示,Mr(KIO3)=214 ).
②在滴定操作正确无误的情况下,用此种测定方法测得的结果往往偏高,其原因是受空气的影响,请用离子方程式表示产生这一影响的原因4I-+O2+4H+=2I2+2H2O.

13.甲烷和乙烯的混合气体100mL,能催化加氢气30mL,则混合气体中含有甲烷( )
| A. | 50mL | B. | 70mL | C. | 30mL | D. | 15mL |
3.具有一个醇羟基的有机物A 与7g乙酸在一定条件下反应后生成10.2g的乙酸某酯,经分析还有1g 乙酸剩余,则A的结构简式可能是( )
| A. | CH3CH2OH | B. | CH3CH2CH2OH | C. | HOCH2CH2CHO | D. | 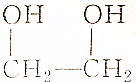 |
10.导致大气污染有很多非金属元素及其化合物,如硫,氮,碳的氧化物及破坏臭氧层的氯等,下列有关氧、硫、碳、氮、氯等非金属元素的各项比较,正确的是( )
| A. | 在常见的化合物中,最高价态从低至高的顺序是:C<N<O=S<Cl | |
| B. | 原子序数从小到大是:C<N<O<S<Cl | |
| C. | 排在元素周期表中所属的主族序数从大至小的是:Cl>O>S>N>C | |
| D. | 原子的最外层电子数由多至少的顺序是:Cl>O=S>N>C |
7.下列物质加入或通入溴水中,水层不能变成无色或接近无色的是( )
| A. | 镁粉 | B. | 碘化钾 | C. | 苯 | D. | 四氯化碳 |