题目内容
【题目】(1)氨的水溶液显弱碱性,其原因为___________________(用离子方程式表示), 0.1 molL-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度__________(填“增大”或“减小”);
(2)25℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________;
②0.10molL-1Na2SO3溶液中离子浓度由大到小的顺序为___________________;
③H2SO3溶液和NaHCO3溶液反应的离子方程式为___________________;
(3)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×10-10,若向5mL0.018molL-1的AgNO3溶液中加入5mL0.020molL-1的盐酸,混合后溶液中的Ag+的浓度为______molL-1,pH为________。
【答案】 NH3H2O![]() NH4++OH- 降低 增大
NH4++OH- 降低 增大 ![]() c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+) H2SO3+HCO3-=HSO3-+CO2↑+H2O 1.8×10-7 2
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+) H2SO3+HCO3-=HSO3-+CO2↑+H2O 1.8×10-7 2
【解析】(1)一水合氨为弱碱,在水溶液中存在部分电离,电离出氢氧根离子使溶液显碱性,方程式为:NH3H2ONH4++OH-,向氨水中加入少量NH4Cl固体,铵根浓度增大,平衡左移,即氢氧根浓度减小,pH值降低,加入少量明矾,明矾电离出的铝离子结合氢氧根生成氢氧化铝,促进氨水的电离,铵根浓度增大;
(2)①HSO3-的电离平衡常数表达式K=![]() ;②Na2SO3溶液显碱性,SO32-存在两步水解:SO32-+H2OHSO3-+OH-,HSO3-+H2OH2SO3+OH-,以第一步水解为主,水解程度较小,则0.1mol/L Na2SO3溶液中的离子浓度顺序为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),故答案为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);③由表可知H2SO3的二级电离小于H2CO3的一级电离,所以酸性强弱H2SO3>H2CO3>HSO3-,所以反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O;
;②Na2SO3溶液显碱性,SO32-存在两步水解:SO32-+H2OHSO3-+OH-,HSO3-+H2OH2SO3+OH-,以第一步水解为主,水解程度较小,则0.1mol/L Na2SO3溶液中的离子浓度顺序为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),故答案为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);③由表可知H2SO3的二级电离小于H2CO3的一级电离,所以酸性强弱H2SO3>H2CO3>HSO3-,所以反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O;
(3)n(AgNO3)=0.05L×0.018mol/L=0.0009mol,n(HCl)=0.05L×0.020mol/L=0.001mol,硝酸银和HCl发生反应AgNO3+HCl=AgCl↓+HNO3,根据方程式知,HCl剩余,混合溶液中c(Cl-)=![]() mol/L=10-2 mol/L,溶液中c(Ag+)=
mol/L=10-2 mol/L,溶液中c(Ag+)=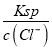 =
=![]() mol/L=1.8×10-8mol/L;实际上氢离子不参加反应,则溶液中c(H+)=
mol/L=1.8×10-8mol/L;实际上氢离子不参加反应,则溶液中c(H+)=![]() =0.1mol/L,溶液的pH=-lgc(H+)=-lg0.1=1,故答案为:1.8×10-8;1;
=0.1mol/L,溶液的pH=-lgc(H+)=-lg0.1=1,故答案为:1.8×10-8;1;


