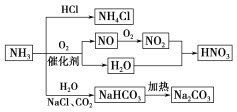
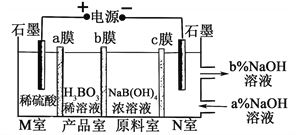
��Ŀ����
����Ŀ�������£���0.10mol��L-1��NaOH��Һ�ֱ�ζ������Ϊ50.00mL��Ũ�Ⱦ�Ϊ0.05mol��L-1��HClO��HF������Һ����ζ�������ͼ��ʾ��
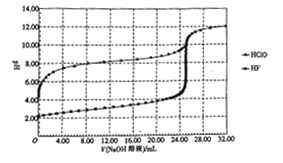
����˵����ȷ����
A. HClO�����Ա�HFǿ
B. V(NaOH��Һ)=0 mL ʱ����Ӧ��Һ�У�c(ClO-)=c(F-)
C. V(NaOH��Һ)=12.50 mL ʱ����Ӧ��Һ�У�c(ClO-)>c(F-)
D. V(NaOH��Һ)=25.00mLʱ����Ӧ��Һ�У�c(ClO-)<c(F-)
���𰸡�D
��������A,��ͼ����Կ�����ͬ��0.10mol/L��һԪ�ᣬHClO��pHԼΪ2����HF��pHԼΪ4������HF���Ա�HClOǿ��A����ȷ��B��������������֪��HF���Խ�ǿ�������Ƚϴ�����������F-��Ũ��Ҳ�ϴ�B����C��V(NaOH��Һ)=12.50 mL ʱ������Һ��c(Na+)��ȣ�HF��Һ��pH<7�����ԣ���HClO��Һ��pH>7�Լ��ԣ��ɵ���غ��֪��c(Na+)+c(H+)=c(F-)+c(OH-), c(Na+)+c(H+)=c(ClO-)+c(OH-),����Һ��c(H+)Խ��c(OH-)��ԽС������c(ClO-)<c(F-)������C����D��V(NaOH��Һ)=25.00mLʱ����Ӧ��Һ�����ʷֱ�ΪNaClO��NaF����������ǿ���Σ��������ʵ���Ũ����ͬ������ˮ�����Һ���Լ��ԣ�����Խ��Խˮ���֪��ClO-��ˮ��̶Ƚϴ�����c(ClO-)<c(F-)��D��ȷ��

 ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�����Ŀ��ij��ѧʵ��С��Ϊȷ����������ֽ����Ѵ�����������ͼװ�ý���ʵ�飬��Ӧ�������ͷ�Ӧֹͣ��ʱ�������±���
MnO2 ʱ�� H2O2 | 0.1 g | 0.3 g | 0.8 g |
10 mL 1.5% | 223 s | 67 s | 56 s |
10 mL 3.0% | 308 s | 109 s | 98 s |
10 mL 4.5% | 395 s | 149 s | 116 s |

��ش��������⣺
��1��ʢװ˫��ˮ�Ļ�ѧ���������� ��
��2����μ������װ�õ��������� ��
��3����ͬŨ�ȵĹ������⣬��ֽ��������Ŷ����������������Ӷ�_______����ӿ족���������䡱����
��4����ʵ��Ч���͡���ɫ��ѧ���ĽǶȿ��ǣ�˫��ˮ��Ũ����ͬʱ������________g(� 0.1 g���� 0.3 g���� 0.8 g��) �Ķ�������Ϊ�ϼ�ѡ��
��5��ijͬѧ�����������ݺ���Ϊ����������ͬ�����Ķ�������ʱ��˫��ˮ��Ũ��ԽС������Ҫ��ʱ���Խ�٣��༴�䷴Ӧ����Խ�족�Ľ��ۣ�����Ϊ�Ƿ���ȷ___________(���ȷ���� ����ȷ��)��������___________________________��(��ʾ��H2O2���ܶȿ���Ϊ�������)��
����Ŀ������/H2O2��Һ����������������������
(1)��֪T��ʱ��2SO2(g)+O2(g) ![]() 2SO3(g) ��H1
2SO3(g) ��H1
2H2O2(I)=2H2O(I)+O2(g) ��H2
SO3(g)+H2O(I))=H2SO4(I) ��H3
��SO2(g)+H2O2(I))=H2SO4(I) ��H4=__________ (�ú���H1����H2����H3�Ĵ���ʽ��ʾ)
(2)����[CO(NH2)2]��Һ��NOx��SO2��һ�����ѳ��ʡ���SO2��NOx (N��Լռ90%)ͨ���������������Ϊ7%������Ũ��Ϊ5%�ķ�Ӧ���н��з�Ӧ��
��������SO2����ת��Ϊһ�����Σ��仯ѧʽΪ______________��NO��NO2�����ʵ���֮��1:1��CO(NH2)2��Ӧ����������Ļ�ѧ����ʽΪ_______________��
�ڰ��������(H2NCOONH4)�����ص�ˮ������һ�����İ�����������ں����ܱ������У�������Ӧ��NH2COONH4(s)![]() 2NH3(g)��CO2(g) ��H��ʵ���ò�ͬ�¶���ƽ��ʱ�������Ũ�����±���
2NH3(g)��CO2(g) ��H��ʵ���ò�ͬ�¶���ƽ��ʱ�������Ũ�����±���
�¶�/K | 338 | 343 | 348 | 353 |
ƽ��ʱ�������Ũ��/mol L-1 | 0.36 | 0.48 | 0.60 | 0.72 |
�÷�Ӧ�ġ�H__________(�>����<��)0��348Kʱ���÷�Ӧ��ƽ�ⳣ��K__________________��
(3)�����������䣬��������Һ������H2O2��Һ����ò�ͬ pH�µ���������ѳ�����ʱ��Ĺ�ϵ��ͼ��ʾ��

��NO��H2O2������Ӧ����������ʱ���������뻹ԭ�������ʵ���֮��Ϊ____________��
(2)����ʱ�����pHΪ_________���ڼ��Խ�ǿʱ��NOx�ѳ��ʽ��ͣ���ԭ����___________(��дһ��)��