题目内容
【题目】根据下面的反应路线及所给信息填空 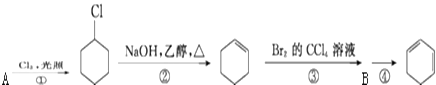
(1)A的结构简式是 , 名称是 .
(2)①的反应类型是 , ③的反应类型是 .
(3)反应④的化学方程式是 .
【答案】
(1)![]() ;环己烷
;环己烷
(2)取代反应;加成反应
(3)![]()
【解析】解:(1.)由反应①可知,A与氯气在光照的条件下发生取代反应生成一氯环己烷,故A为 ![]() ,名称为环己烷,故答案为:
,名称为环己烷,故答案为: ![]() ;环己烷;
;环己烷;
(2.)反应①环己烷中H原子被氯原子取代生成一氯环己烷,该反应为取代反应,反应③是环己烯与溴发生加成反应生成B,故答案为:取代反应;加成反应;
(3.)环己烯与溴发生加成反应生成B为 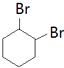 ,故反应④是
,故反应④是  发生消去反应生成
发生消去反应生成 ![]() ,反应方程式为:
,反应方程式为: ![]() ,
,
故答案为: ![]() .
.
(1)由反应①可知,A与氯气在光照的条件下发生取代反应生成一氯环己烷,故A为 ![]() ;(2)反应①环己烷中H原子被氯原子取代生成一氯环己烷;反应③是环己烯与溴发生加成反应生成B;(3)环己烯与溴发生加成反应生成B为
;(2)反应①环己烷中H原子被氯原子取代生成一氯环己烷;反应③是环己烯与溴发生加成反应生成B;(3)环己烯与溴发生加成反应生成B为 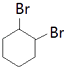 ,故反应④是
,故反应④是  发生消去反应生成
发生消去反应生成 ![]() .
.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
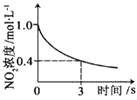
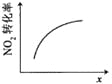
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度, | 0~3s内,反应速率为: | t1时仅加入催化剂, | 达平衡时,仅改变x,则x为c(O2) |