题目内容
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC=![]() vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,vA=________,vB=________。
(2)化学方程式中,x=________,y=__________,p=__________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH________0。(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:
①反应速率________(填“增大”“减小”或“不变”),理由是____________________________。
②平衡时反应物的转化率________(填“增大”“减小”或“不变”),理由是_________________________。
【答案】(1)![]() mol·(L·min)1(3分)
mol·(L·min)1(3分) ![]() mol·(L·min)1(3分)
mol·(L·min)1(3分)
(2)2(2分) 3(2分) 1(2分) 6(2分)
(3)![]() ×100%(3分) (4)<(2分)
×100%(3分) (4)<(2分)
(5)①增大(1分) 体积减小,反应物的浓度增大,因而使反应速率增大(2分)
②减小(1分) 体积减小,气体的压强增大,平衡向气体分子数少的方向(即逆反应方向)移动,因而使反应物转化率减小(2分)
【解析】由 xA(g)+yB(g) ![]() pC(g)+qD(g)
pC(g)+qD(g)
起始(mol) a b 0 0
平衡(mol) a-![]() b-
b-![]() a
a
则x∶y∶q=![]() ∶
∶![]() ∶a=2∶3∶6,而
∶a=2∶3∶6,而![]() =
=![]() =
=![]() =2,故x∶y∶p∶q=2∶3∶1∶6。
=2,故x∶y∶p∶q=2∶3∶1∶6。
(1)vA=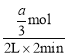 =
=![]() mol·(L·min)-1,vB=
mol·(L·min)-1,vB=![]() vA=
vA=![]() mol·(L·min)-1。
mol·(L·min)-1。
(3)B的转化率为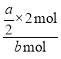 ×100%=
×100%=![]() %。
%。
(4)升温生成物的量减少,即平衡逆向移动,故正反应放热,ΔH<0。
(5)①容器的容积变小,浓度增大,相当于加压,反应速率加快。
②加压平衡向逆反应方向移动,反应物的转化率减小。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案