题目内容
【题目】小华在实验室进行以下实验:将四个完全相同的空心薄铁皮球分别放入四个盛有密度为ρ(g/cm3)的食盐水的烧杯中,铁球所处的位置如图所示。然后,他将水、密度均为ρ(g/cm3)的三种溶液(CuSO4、AgNO3、稀硫酸)分别加入上述四个烧杯中。回答下列问题:
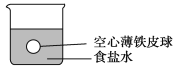
(1)加入水时,看到的现象是____________________________________________。
(2)加入稀硫酸时看到的现象是(假定整个反应过程中铁皮球壁完整)_____________________,发生反应的离子方程式是____________________________________________。
(3)加入CuSO4溶液时看到的现象是___________________________________________________,
发生反应的离子方程式是______________________________________________。
(4)加入AgNO3溶液时看到的现象是_________________________________,发生反应的离子方程式是_____________________________________________________。
【答案】(1)铁球下沉
(2)铁球表面产生气泡并慢慢上浮 Fe+2H+![]() Fe2++H2↑
Fe2++H2↑
(3)铁球表面变红,铁球下沉 Fe+Cu2+![]() Cu+Fe2+
Cu+Fe2+
(4)溶液中有白色沉淀,铁球下沉,继而表面有银白色物质生成 Ag++Cl![]() AgCl↓、Fe+2Ag+
AgCl↓、Fe+2Ag+![]() 2Ag+Fe2+
2Ag+Fe2+
【解析】(1)加入水时,与食盐及铁球不反应,但加水后,溶液密度变小,故小球下沉。
(2)加入稀H2SO4时,虽不能与NaCl反应,但可与铁球发生反应Fe+H2SO4![]() FeSO4+H2↑,铁球质量减小,故小球上浮。
FeSO4+H2↑,铁球质量减小,故小球上浮。
(3)加入CuSO4溶液时,发生反应Fe+CuSO4![]() Cu+FeSO4,生成的铜比溶解的铁质量大且附着在铁球上,故小球下沉。
Cu+FeSO4,生成的铜比溶解的铁质量大且附着在铁球上,故小球下沉。
(4)加入AgNO3后发生反应AgNO3+NaCl![]() AgCl↓+NaNO3,溶液中出现白色沉淀,此溶液发生反应后密度变小,小球下沉,此过程中可能发生反应Fe+2AgNO3
AgCl↓+NaNO3,溶液中出现白色沉淀,此溶液发生反应后密度变小,小球下沉,此过程中可能发生反应Fe+2AgNO3![]() Fe(NO3)2+2Ag,而使铁球表面析出银白色物质。
Fe(NO3)2+2Ag,而使铁球表面析出银白色物质。