题目内容
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品,易溶于水,遇酸易分解,Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成。工业制备Na2S2O3的反应为: S(s)+Na2SO3(aq)![]() Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。
Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。

请回答下列问题:
(1)按如图所示装置进行实验,装置A中反应的化学方程式是______________________。装置C中可观察到溶液先变浑浊,后又澄清,生成的浑浊物质化学式为___________。
(2)装置B的作用为_________;为保证Na2S2O3的产量,实验中通入的SO2不能过量,原因是_________。
(3)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:
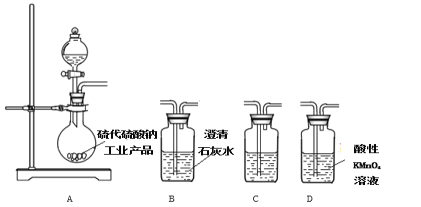
①实验装置的连接顺序依次________________(填装置的字母代号),装置C中的试剂为____________。
②能证明固体中含有碳酸钠的实验现象是__________________。
(4)若要检验固体硫代硫酸钠工业产品中含有Na2SO3,需先加水配成稀溶液,再依次加入的试剂为_____________________和品红溶液。
【答案】
(1)Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;S;
(2)防止溶液倒吸;若SO2过量,溶液显酸性,产物会分解
(3)①ADCB;品红溶液;②装置C中品红溶液不褪色,B中澄清石灰水变浑浊
(4)氯化钡溶液、盐酸
【解析】(1)装置A中浓硫酸与亚硫酸钠反应生成二氧化硫,反应的化学方程式为Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;二氧化硫能够与硫化钠在酸性溶液中发生氧化还原反应,生成硫单质,生成的硫有发生S(s)+Na2SO3(aq)![]() Na2S2O3(aq),因此装置C中可观察到溶液先变浑浊,后又澄清,故答案为:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;S;
Na2S2O3(aq),因此装置C中可观察到溶液先变浑浊,后又澄清,故答案为:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;S;
(2)装置B是安全瓶。可以防止溶液倒吸;根据题意,若SO2过量,溶液显酸性,产物Na2S2O3会分解,故答案为:防止溶液倒吸;若SO2过量,溶液显酸性,产物会分解;
(3)碳酸钠能够与酸反应生成二氧化碳,可以利用澄清石灰水检验,但由于混有二氧化硫,因此须用高锰酸钾溶液除去二氧化硫,并检验,实验装置的连接顺序依次为ADCB,装置C中的作用是检验二氧化硫是否除净,因此选用的试剂为品红溶液,故答案为:ADCB;品红溶液;
②能证明固体中含有碳酸钠的实验现象是装置C中品红溶液不褪色,B中澄清石灰水变浑浊,故答案为:装置C中品红溶液不褪色,B中澄清石灰水变浑浊;
(4)根据题意,Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成,若要检验固体硫代硫酸钠工业产品中含有Na2SO3,需先加水配成稀溶液,再依次加入的试剂为氯化钡溶液、盐酸和品红溶液,若加入氯化钡溶液生成白色沉淀,过滤后,白色沉淀能够被盐酸溶解,放出的气体能够使品红溶液褪色,证明固体硫代硫酸钠工业产品中含有Na2SO3,故答案为:氯化钡溶液、盐酸。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案