题目内容
【题目】探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是
A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水
B.将pH=11的氨水稀释1000倍,测得pH > 8,说明NH3·H2O为弱碱
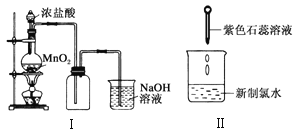
C.加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定
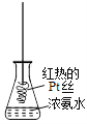
D.将红热的Pt丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为NO2
【答案】D
【解析】本题考查对氨气和铵盐性质的判断。A、将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水,使试管内的压强迅速减小,水充满试管,正确;B、若一水合氨是强碱,将pH=11的氨水稀释1000倍,pH = 8,现在测得pH > 8,说氨水中存在一水合氨的电离平衡,稀释促进电离,所以溶液的pH降低程度减小,正确;C、加热NH4HCO3固体,固体逐渐减少,试管口有液滴产生,说明有水生成,所以可以说明NH4HCO3受热不稳定,分解为氨气、二氧化碳、水,正确;D、挥发的氨气在红热的Pt丝作催化剂的条件下和O2发生催化氧化反应生成的NO遇到O2又生成红棕色的NO2。所以瓶口出现红棕色气体,错误。所以选D。

练习册系列答案
相关题目