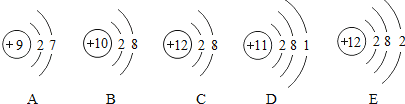【题目】科学探究是奇妙的过程,请你一起参与实验探究。
(提出问题)不同的氧化物在氯酸钾制取氧气实验中能否起催化作用
(设计实验)按下表完成实验
实验编号 | 氯酸钾质量 | 氧化物 | 产生气体的体积 | 耗时 |
1 | 0.6g | / | 9.8mL | 480s |
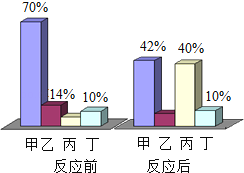
2 | 0.6g | 0.2g二氧化锰 | 67mL | 36.5s |
3 | 0.6g | 0.2g氧化铁 | 67mL | 89.5s |
(1)写出实验2反应的化学方程式_____;
(2)测量实验3中氧气的体积,所需的量筒规格为_____(选填“10”、“50”或“100”)mL;
(3)为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g;
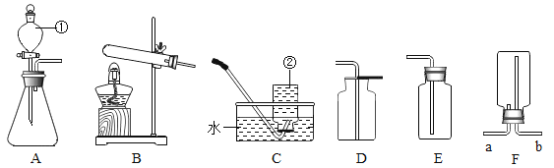
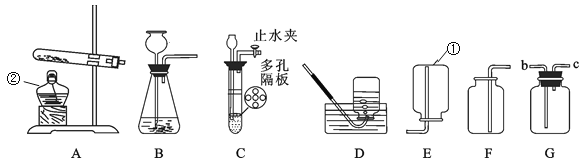
Ⅱ将过量的CO通入滤出的固体,按下图所示装置进行实验,并分析研究。
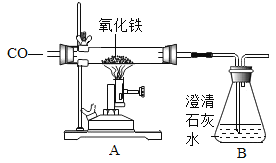
甲同学的实验报告如下:
装置 | 现象 | 结论 |
A | 红色固体全部变黑 | 生成了铁 |
B | ______ | 产生了二氧化碳 |
A处的化学方程式:_____。
(实验结论)以上实验证明氧化铁能作为氯酸钾受热分解的催化剂。两种氧化物相比,_____(选填“二氧化锰”或“氧化铁”)的催化效果好。
(定量计算)若该实验玻璃管中的固体质量减少了0.03克,求:(写出计算过程)
①氧化铁的质量?_____
②生成多少克的铁?_____
(交流反思)上图所示实验装置存在不足之处,理由是_____。
【题目】目前,我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础。
(一)铁的广泛应用
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由_________构成。我国在西汉时期就有“曾青得铁则化为铜”之说,其化学方程式是______________________。
(2)生活中:右图是常用的铁锅。用铁锅做炊具,是利用了铁的___________性。防止铁锅生锈,通常采用的方法是____________。

(3)实验室:铁丝在纯净氧气中燃烧的化学反应方程式为__________。铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是___________(填化学式)。
(二)铁锈蚀的条件探究
(4)铁在潮湿的空气里容易发生锈蚀,证明水一定参加了反应,必须要做的对比实验是_______(填字母)。
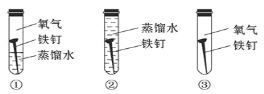
A.①② B.①③ C.②③ D.①②③
(5)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性强的金属首先被腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的是_____(填“锌块”或“铜块”)。
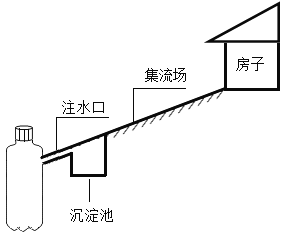
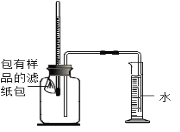
(6)如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为150mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如下表。(滤纸包等所占体积忽略不计)
序号 | 样品 | 量筒起始读数 | 量筒最终读数 | 所需时间/min |
1 | 1g铁粉、0.2 g碳和10滴水 | 100 mL | 72 mL | 约120 |
2 | 1g铁粉、0.2g碳、10滴水和少量NaCl | 100 mL | 72 mL | 约70 |
3 | / | / | / |
①铁锈的主要成分是______(写化学式)。
②实验1和2说明NaCl可以_______(填“加快”或“减慢”)铁锈蚀的速率。
③实验开始后广口瓶内温度上升,说明铁锈蚀过程是______(填“放热”或“吸热”)过程。④实验1和3是探究碳对铁锈蚀速率的影响,表格空白处应填写的实验3的样品组成是________。
⑤该装置还可用于测量空气中氧气的体积分数。根据上述数据计算氧气的体积含量是________%(精确到小数点后1位)。
(三)铁的冶炼
(7)某钢铁厂炼铁的主要原料是焦炭、赤铁矿(主要成分为氧化铁)、石灰石等,炼铁设备--高炉结构如图所示,请回答下列问题:
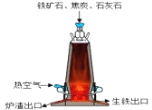
①炼铁的固体原料需预先经过粉碎,其目的是___________。
②炼铁高炉内发生的主要过程如下:
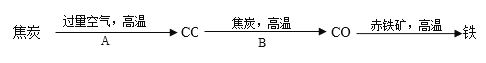
写出步骤写出A、B两步反应的化学方程式:
A:_____________,B:________________
③资料显示,炼铁中焦炭的实际用量远高于理论值,可能原因是______(填字母)。
A.部分焦炭与铁相互熔合,成为生铁中的部分碳元素
B.焦炭转变成一氧化碳后,并不能全部参加反应
C.焦炭在高温下会分解
④某炼铁厂现用100t含氧化铁80%的赤铁矿石炼铁,计算理论上可以炼出含铁96%的生铁的质量__________span>。(计算结果精确到0.1t)