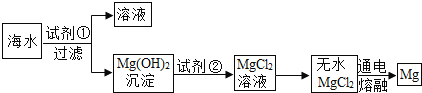
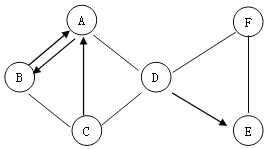
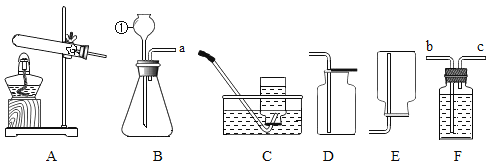
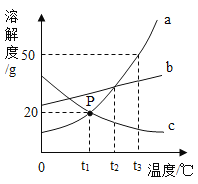
【题目】某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
[提出问题]澄清石灰水为什么没有变浑浊?
[查阅资料]
(1) CO2过量时,CaCO3沉淀会转化为可溶于水的Ca (HCO3)2。
(2)AgCl不溶于稀硝酸
[提出猜想] I.石灰水已完全变质;
II.CO2过量;
III.CO2中混有 HCl。
[实验方案]兴趣小组用原药品继续制取CO2,并进行探究。
制备CO2的化学方程式______________。
[实验结论]制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
[交流讨论]若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和____________。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入______溶液。 | 产生白色沉淀。 | 猜想I不成立 |
(2) | 将少量气体通入盛有澄清石灰水的试管中。 | ______________。 | 猜想Ⅱ不成立 |
(3) | 将气体通入盛有_______溶液的试管中,再加稀硝酸。 | _______________。 | 猜想III成立,反应方程式为___________。 |
【题目】化学小组取形状和大小均相同的镁片,锌片,铝片、铁片,分别与5%的稀硫酸反应,测得反应速度由大到小的顺序是:镁>锌>铁>铝。为什么实验结果与金属活动性顺序不完全一致呢?小组同学猜想可能的原因,设计了如下探究实验。(说明:实验中所用酸的体积相等且足量)
实验序号 | 操作 | 反应速度 | |
Ⅰ | 取形状和大小均匀相同的镁片、铝片、铁片、锌片,________。放入试管中,分别同时加入 | 5%的稀硫酸 | 镁>锌>铁>铝 |
Ⅱ | 10%的稀硫酸 | 镁>锌>铁>铝 | |
Ⅲ | 5%的稀盐酸 | 镁>铝>锌>铁 | |
Ⅳ | 10%的稀盐酸 | 镁>铝>锌>铁 | |
(1)上述实验中横线处的操作是__________。设计实验Ⅰ、Ⅱ的目的是____________________。
(2)对比实验_____(填序号),初步判断铝与酸反应的速度在排序中出现变化的原因可能与_____有关,某同学向铝与不同浓度稀硫酸反应的试管中加入等量氯化钠固体,发现反应速度均明显变快,从微观角度分析,原因是_______________。
(3)实验后,同学们绘制了本次探究实验中铝与稀盐酸反应的下列图象,其中正确的是_____(填字母序号),判断依据为____________________。
A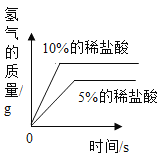 B
B 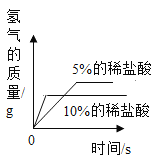 C
C
【题目】实验室有五瓶没有标签的无色溶液,分别是稀盐酸、氢氧化钙溶液、氢氧化钠溶液、碳酸钠溶液和酚酞溶液。为确定溶液组成,化学小组将五瓶溶液编号为A、B、C、D、E并进行如下实验。
实验 |
|
|
|
|
现象 | 无明显现象 | 溶液变红 | 产生气体 | 溶液变红 |
(1)酚酞溶液的编号是_____。
(2)上述实验无法鉴别出的溶液名称是_____;利用现有试剂,继续鉴别,写出操作步骤、现象和结论。_____。
(3)甲、乙两个小组分别进行上述实验后,将实验过程中所有溶液倒入自己小组的废液缸。
甲组观察到废液缸中只有无色溶液,其中溶质的组成为_____ (不写酚酞,下同);
乙组观察到废液缸中溶液呈红色且浑浊,符合该现象最简单的溶质的组成为__________ 。