题目内容
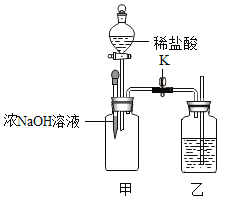
【题目】某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
[提出问题]澄清石灰水为什么没有变浑浊?
[查阅资料]
(1) CO2过量时,CaCO3沉淀会转化为可溶于水的Ca (HCO3)2。
(2)AgCl不溶于稀硝酸
[提出猜想] I.石灰水已完全变质;
II.CO2过量;
III.CO2中混有 HCl。
[实验方案]兴趣小组用原药品继续制取CO2,并进行探究。
制备CO2的化学方程式______________。
[实验结论]制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
[交流讨论]若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和____________。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入______溶液。 | 产生白色沉淀。 | 猜想I不成立 |
(2) | 将少量气体通入盛有澄清石灰水的试管中。 | ______________。 | 猜想Ⅱ不成立 |
(3) | 将气体通入盛有_______溶液的试管中,再加稀硝酸。 | _______________。 | 猜想III成立,反应方程式为___________。 |
【答案】![]() 浓硫酸 碳酸钠 溶液不变浑浊 硝酸银 产生白色沉淀
浓硫酸 碳酸钠 溶液不变浑浊 硝酸银 产生白色沉淀 ![]()
【解析】
[实验方案]石灰石主要组分为碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,据此书写化学方程式;
故答案为:![]() 。
。
[交流讨论]制取干燥二氧化碳,需要去除水蒸气,可以利用浓硫酸吸水性干燥气体;
故答案为:浓硫酸。
(1)实验结论为猜想Ⅰ不成立,说明未发生变质,澄清石灰水含有氢氧化钙,可以加入碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,观察到白色沉淀;
故答案为:碳酸钠。
(2)通入少量气体,说明二氧化碳是不足量,而结论为猜想Ⅱ不成立,说明此时也不产生沉淀,不产生浑浊现象,从而排出二氧化碳用量的影响;
故答案为:溶液不变浑浊。
(3)实验结论为猜想Ⅲ成立,因此说明气体中混有氯化氢,气体通入溶液中形成盐酸,盐酸中含有氯离子,氯离子与银离子可以反应生成氯化银沉淀,因此可以加入硝酸银溶液,观察到白色沉淀,证明氯离子存在,从而推出气体中含有氯化氢;氯化氢与硝酸银反应生成硝酸和氯化银沉淀,据此书写化学方程式;
故答案为:硝酸银;产生白色沉淀;![]() 。
。