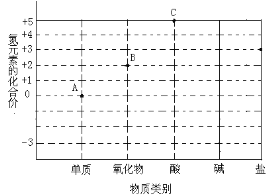
【题目】(1)小明用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和 pH 的变化。测定结果如图所示。根据图示回答下列问题:

氢氧化钠和盐酸的反应属于______填“吸热”或“放 热”)反应。写出 61s 时,溶液中溶质的化学式_____。
(2)某化学小组用一定量的 AgNO3 和 Cu(NO3)2 的混合溶液进行了如图所示的实验,并对溶液 A 和固体 B 的成分进行了分析和实验探究。

(提出问题)溶液A中的溶质成分可能有哪些?
(做出猜想)猜想①:只有 Zn(NO3)2;
猜想②:有 Zn(NO3)2、Cu(NO3)2;
猜想③: 有 Zn(NO3)2、AgNO3;
猜想④:有 Zn(NO3)2、Cu(NO3)2、AgNO3
(交流讨论)不合理的猜想是_____(填序号),其理由是_____。
(实验探究)若猜想①成立,通过以下实验可确定固体的成分,请将下表填写完整
实验步骤 | 现象 | 有关反应的化学方程式 |
取少量固体,滴加_____ | 有气泡产生 | _____ |
(深入思考)若猜想④成立,固体 B 的成分是_____。
(3)除去 NaCl 溶液中 CaCl2 、MgCl2、Na2SO4 杂质的操作:①加过量的 NaOH 溶液;②加过量的 BaCl2 溶液;③过滤;④加适量的盐酸;⑤加过量的 Na2CO3 溶液。
(提示:Mg(NO3)2、BaSO4、BaCO3 难溶于水)写出以上操作的合理顺序_____(数字序号不能重复使用)。请写出溶液 BaCl2 与 Na2SO4 溶液反应的化学方程式_____。
(4)上述试剂中的 Na2CO3 溶液不能用 K2CO3 溶液代替,请说明原因_____。
【题目】(1)用化学用语填空:保持氨气化学性质的微粒是_____;配制农药波尔多液所用硫酸 铜的构成粒子是_____;试写出一种常见化学复合肥料主要成分的化学式_____。
(2)一些食物的近似 pH 如下表:
食物 | 苹果 | 葡萄 | 牛奶 | 玉米粥 |
pH | 2.9-3.3 | 3.5-4.5 | 6.3-6.6 | 6.8-8.0 |
苹果汁和葡萄汁相比较,酸性较强的是(_______),它能使紫色石蕊试液变成(_______) 色。人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜使用上述食物中的(_______)。在 医疗上,治疗胃酸过多的药物之一是碳酸氢钠,请写出它与胃酸中的盐酸反应的化学方程式(______) 。
(3)氮气的一种常见实验室制法是用氯化铵(NH4Cl)与亚硝酸钠(NaNO2)反应,同时生成氯化钠和水。写出该反应的化学方程式:(______)。
(4)如图是甲、乙两种固体的溶解度曲线。

t1℃时,若甲溶液中溶质与溶剂的质量比为 1:5,则该溶液属于_____(选填“饱和”或“不饱和”)溶液;t2℃时,将 60g 甲的饱和溶液稀释成 10%,需加水_____;将 t2℃时甲、乙的饱和溶液降温至 t1℃(其他条件不变),所得溶液的溶质质量分数关系为:甲_____(选填“〉”、“〈”或“=”)乙。