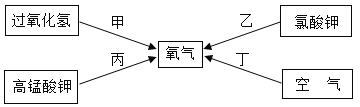
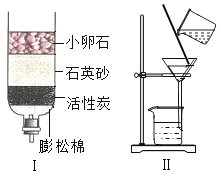
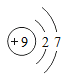【题目】某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为_____.
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的____和_______都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
I | 50.0g | 1% | 0.1g | 9mL |
II | 50.0g | 2% | 0.1g | 16mL |
III | 50.0g | 4% | 0.1g | 31mL |
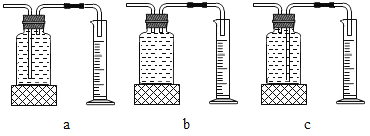
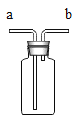
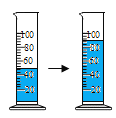
①若用上述装置测生成氧气的体积,则用图___(填“a”“b”或“c”)
②实验结论:在相同条件下,______________,双氧水分解得快.
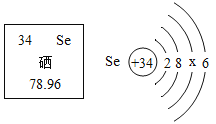
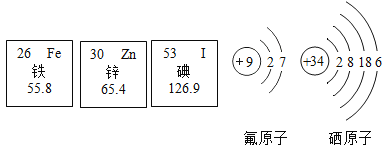
【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题:
IA | 0 | |||||||
1 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
IIA | IIIA | IVA | VA | VIA | VIIA | |||
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
请根据相关信息与知识回答:
(1)1869年,_____(填序号)发现了元素周期律并编制了元素周期表;
A 拉瓦锡 B 张青莲 C 门捷列夫 D 道尔顿和阿伏加德罗
(2)请从上表中查出地壳中含量最多的金属元素的相对原子质量为_____。
(3)表中不同种元素最本质的区别是_____(填序号):
A 相对原子质量不同 B 质子数不同 C 中子数不同
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:_____(填字母序号)
A 从左到右,各元素原子的电子层数相同
B 从左到右,各元素原子的最外层电子数依次增加
C 从左到右,各元素原子的最外层电子数相同
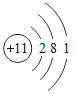
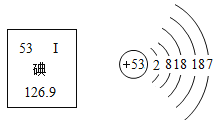
(5)元素周期表中,原子序数为12的镁元素的原子结构示意图如图,该原子在化学反应中易_____(填“得到”或“失去”)电子,其离子符号为_____。说明元素的化学性质与原子的_____关系密切。

【题目】对下列实验现象的解释错误的是
A | B | C | D | |
实验现象 |
用扫描隧道显微镜获得的分子图像 |
品红加入水中后,整个液体变红色 |
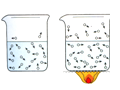
水分子在不同温度下的运动情况 |
50mL水与50mL酒精混合后的体积小于100mL |
解释 | 分子的质量和体积都很小 | 分子总是不断的运动着的 | 常温时分子不运动,加热时分子才运动 | 分子有空隙 |
A.AB.BC.CD.D
【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化作用呢?于是该同学进行了以下探究。
(猜想)
I.氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了变化;
Ⅲ.氧化铜是反应的催化剂,反应前后_____________。
(实验)用天平称量0.2g氧化铜,取5m5%的过氧化氢溶液于试管中,进行如下实验:
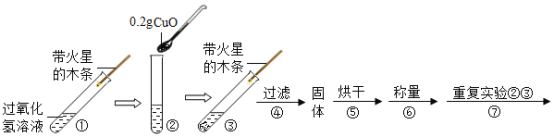
(1)猜想Ⅲ中,氧化铜是反应的催化剂,反应前后________。
(2)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
__________,带火星的木条复燃 | __________ | 溶液中有气泡放出 | 猜想I、Ⅱ不成立,猜想Ⅲ成立 |
(3)步骤①的目的是_______________。
(4)步骤⑦的目的是____________。
(5)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为__________