【题目】下列有关化学知识的说法正确的是
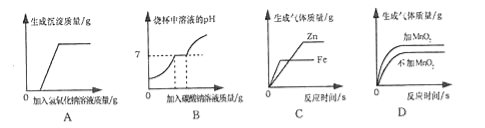
A.可燃物只要温度达到着火点就能燃烧
B.常温下所有金属都是银白色的固体
C.大多数固体物质的溶解度随温度的升高而增大
D.铁丝浸没在水中比暴露在潮湿的空气中更容易生锈
【题目】某工业铁红(Fe2O3)样品中可能混有一种黑色的金属氧化物杂质。根据工业制取铁红的流程分析,该杂质可能是FeO或CuO。兴趣小组同学为探究样品中是否含有杂质及杂质的成分,进行如下实验。
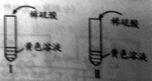
(1)甲组同学分别取质量相等的样品和Fe2O3,加入试管Ⅰ、Ⅱ中,然后加入等体积稀硫酸进行如图对照实验,并得出结论:样品中不含杂质。你认为该结论_______(填“合理”或“不合理”)。
(2)乙组同学按下列步骤进行实验:
【收集资料】
①上述三种氧化物在加热条件下,都能与氢气反应得到相应的金属单质和水。
②三种氧化物中氧元素的质量分数由大到小的顺序为____________。
③铁粉中混有少量铜时,难以从金属颜色确定是否含有金属铜。
【设计方案进行实验】
乙组同学用下图装置进行实验(碱石灰是氧化钙与氢氧化钠固体混合物)。

①乙组同学的实验装置中,依次连接的合理顺序为A→F→_____→_______→______→B。检验装置气密性后,向各装置中加入药品。装置F中试剂X是_____溶液,装置C的作用是___________。
②下列实验操作步骤的合理顺序是________(填写操作编号)。
a.加热装置D中反应管 b.检验H2的纯度
c.打开装置A中分液漏斗的活塞,向圆底烧瓶中加入稀盐酸
③该实验处理问起的方法是______________。
【实验分析与结论】
乙组同学的两次实验数据如下表:(两次实验工业铁红均与氢气完全反应)
实验编号 | 加入装置D中工业铁红的质量(g) | 实验后装置E的增重(g) |
1 | 8.0 | 2.6 |
2 | 16.0 | 5.2 |
①分析数据,你的实验结论是_________________。
②请帮助乙组同学设计实验方案确认该样品中杂质的成分________________。(写出操作、现象和结论,若该样品中不含杂质本题不必作答)
【题目】实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸的质量分株,进行如下探究:
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。实验数据如下表所示:
实验序号 | 所取样品质量(g) | 所加盐酸质量(g) | 生成氢气质量(g) |
Ⅰ | 16.0 | 60.0 | 0.5 |
Ⅱ | 16.0 | 130.0 | 1.0 |
Ⅲ | 16.0 | 150.0 | 1.0 |
镁粉样品中金属镁的质量百分含量为_________________。
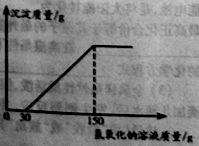
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠溶液质量的变化关系如图所示。计算盐酸的质量分数。(写出计算过程)