【题目】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于酸)为原料制备高纯氧化镁的实验流程如下:
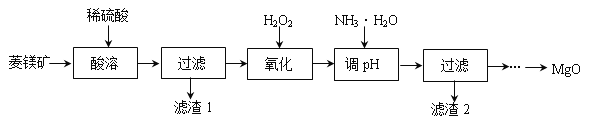
(1)酸溶之前要将矿石粉碎的目的是 。稀硫酸需要过量的目的是 。酸溶步骤中碳酸镁溶解的反应方程式为 。
(2)已知Mg2+、Fe2+和Fe3+在溶液中遇到氨水均可以转化成难溶性碱沉淀,开始沉淀和沉淀完全的pH如下表:
Mg2+ | Fe2+ | Fe3+ | |
开始沉淀 | 9.4 | 7.9 | 2.7 |
沉淀完全 | 12.4 | 9.6 | 3.7 |
流程“氧化”一步中H2O2的作用是将溶液中的Fe2+转化成Fe3+,不能直接沉淀Fe2+的原因是 。
(3)加氨水调节溶液的PH范围为 。
(4)滤渣2的化学式是 。
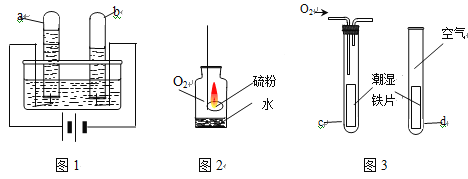
【题目】实验室利用下图实验装置进行有关化学实验,请回答下列问题:
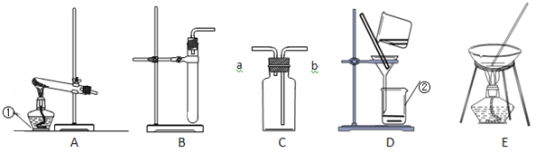
(1)写出图中指定仪器的名称:① ;② 。
(2)实验室用氯酸钾和二氧化锰制取氧气,发生装置可选择图中的 (填字母),该反应的化学方程式为: 。
(3)某同学想通过装置C收集二氧化碳,气体应从 (填“a”或“b”)进入。
(4)对上述制取二氧化碳实验后的固液残留物进行分离,可选择上图中的装置 (填字母),该操作中玻璃棒的作用是 。
(5)某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 充分反应后 | ||
实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
180 g | 12g | 187.6g | |
求该石灰石中碳酸钙的质量分数。(计算结果保留一位小数)