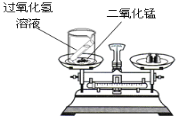
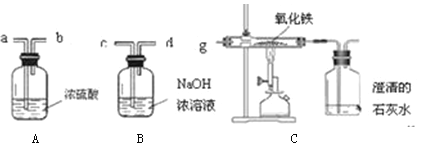
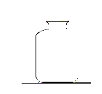
【题目】(8分)小明设计了如下图所示的实验装置来证明氧化铜也能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30 mL气体为准(即比较反应的快慢程度)。
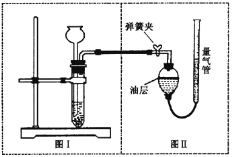
用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
实验序号 | 过氧化氢溶液体积 | 催化剂 | 待测数据 |
① | 15mL | 无 | |
② | 15mL | CuO(0.5g) | |
③ | 15mL | MnO2(0.5g) |
(1)检查图(Ⅰ)装置气密性的方法是: ;
实验②操作时图(Ⅰ)装置中加入药品和试剂的先后顺序是, (用化学式填写);
(2)图(Ⅱ)装置中油层的作用是阻止氧气与水的接触,防止氧气 。
(3)从设计原理看,实验中的“待测数据”是指 。
(4)如果要进一步探究CuO是否是该反应的催化剂,根据催化剂的定义,请完成下列实验。
实验步骤和现象 | 设计这一步骤的目的 |
(1)取15mL过氧化氢溶液,加入0.5g CuO后,产生O2的速率比未加入时快得多 | CuO能加快过氧化氢溶液的分解 |
| |
【题目】向烧杯中逐滴加入x溶液至过量,反应过程中生成沉淀或气体的质量与加入x溶液的质量关系能用下图所示的曲线表示的是


序号 | 烧杯中的物质 | x溶液 |
① | 铜锌合金 | 稀HCl |
② | 盐酸与稀硫酸 | Na2CO3溶液 |
③ | 生锈的铁钉 | 稀HCl |
④ | H2SO4和CuSO4溶液 | NaOH溶液 |
A.①② B.②③④ C.①②④ D.③④