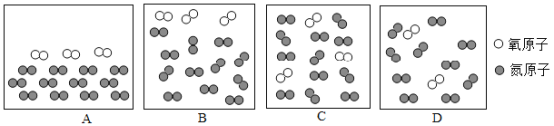
为除去下列物质中的杂质,下列操作方法能达到目的的是
选项 | 物质(杂质) | 操作方法 |
A | CO2气体(H2O) | 将气体通过盛有足量火碱的干燥管 |
B | CuO固体(CuSO4) | 加入过量稀硫酸并加热 |
C | FeCl2溶液(CuCl2) | 加入过量的铁粉,振荡,过滤 |
D | Na2SO4溶液(Na2CO3) | 加稀盐酸至恰好不再产生气泡为止 |
A.A B.B C.C D.D
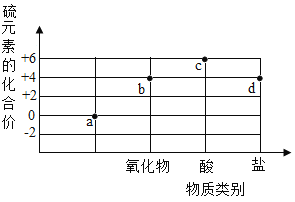
下列实验中,现象与结论对应关系正确的是
实验 | 现象 | 结论 | |
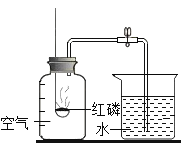
A |
| 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约1/5 | 氧气约占空气质量的1/5 |
B |
| 铜片上的白磷燃烧,热水中的白磷不燃烧 | 燃烧需要达到可燃物的着火点 |
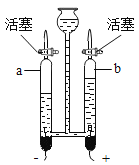
C |
| a中的气体能燃烧,产生淡蓝色火焰,b中的气体能使燃着的木条燃烧更旺 | 水是由氧气和氢气组成 |
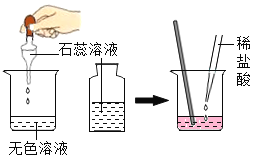
D |
| 滴有紫色石蕊的溶液呈蓝色,加入稀盐酸后蓝色变为红色 | 反应后的溶液中一定不含碱性物质 |
A.A B.B C.C D.D
某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验。

编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)仪器①的名称为____________。
(2)实验室用KClO3制取氧气的化学方程式为_______________________________。
(3)表中所列3种催化剂的催化效果最佳的是____________。
(4)由实验1和实验4可知,KCl对KClO3分解______(填“有”或“无”)催化作用。
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内____________。
某课外兴趣小组的同学对二氧化碳的制取和性质进行相关探究。
(实验回顾)(1)实验室用大理石与稀盐酸制取二氧化碳的化学方程式为_______________。
(2)下图可用于实验室制取CO2发生装置的是__________(填字母)。
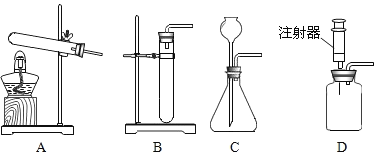
(实验探究)CO2与NaOH溶液反应
(查阅资料)
(1)过量CO2通入NaOH溶液,发生两步反应。
第一步:____________________________(用化学方程式表示)
第二步:Na2CO3+H2O+CO2=2NaHCO3
(2)Na2CO3和NaHCO3部分溶解度表
温度/℃ | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
NaHCO3/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
Na2CO3/g | 7.1 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
(实验设计)在室温为15℃时,将10gNaOH固体完全溶解于80g水中,而后匀速通入CO2,同时用传感器测定溶液的pH变化,结果如图1所示。多次重复实验,所得实验结果基本一致。
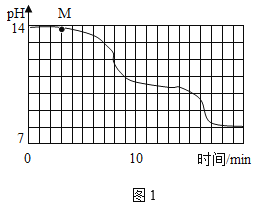
(1)通过图像分析,NaHCO3溶液显_____(填“酸性”、“中性”或“碱性”)。
(2)为了确定M点溶液的成分,同学们进行如下实验:
实验步骤 | 实验现象 | 初步实验结论 |
①取样,滴加过量的BaCl2溶液 | 产生白色沉淀 | 含有Na2CO3、NaOH |
②在①反应后的上层清液中滴加____ | _____ |
(3)实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时溶液中可观察到的现象是______________________________。
(拓展延伸)某同学向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的稀盐酸,测得消耗盐酸与生成CO2的质量之间关系如图2、图3所示。(忽略CO2在水中的溶解)
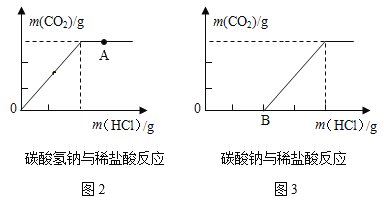
(1)图2中A点溶液中的溶质是_________(写化学式 ),图3中从B点开始的变化关系与图2完全重合,图3中B点溶液中的溶质是__________(写化学式)。
(2)写出OB段发生反应的化学方程式______________________________。