题目内容
【题目】如表为元素周期表中部分元素的相关信息,请利用如表回答相关问题。
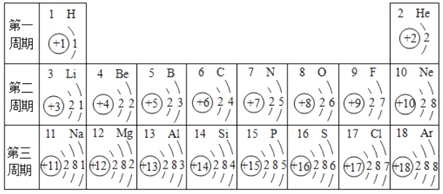
(1)碳原子的核电荷数是_____。
(2)12号元素的原子在化学反应中比较容易_____(填“得到”或“失去”)电子。
(3)在同一周期中,从左到右各元素的原子最外层电子数逐渐_____。
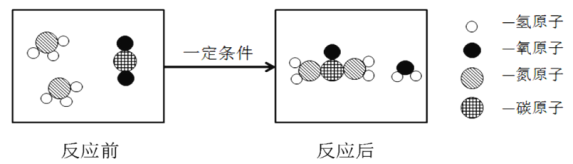
(4)一定条件下,将2.4gCH4与8.0g由8号元素组成的单质,在点燃条件下恰好完全反应,生成5.4gH2O、2.2gCO2和物质X,该化学方程式为3CH4+5O2![]() CO2+6H2O+2X,则X的化学式是_____。
CO2+6H2O+2X,则X的化学式是_____。
(5)将镁、钙、铁、铜四种等质量的金属投入到足量的稀硫酸中,反应速度最快的是_____,产生氢气最多的是_____。
【答案】6; 失去 增加 CO 镁; 镁
【解析】
(1)根据元素周期表可知碳原子的原子序数为6,由原子序数=核电荷数,因此碳原子的核电荷数为6;故答案为:6;
(2)12号元素原子最外层电子数是2,在化学反应中其原子比较容失去到2个电子变成离子;12号元素是镁,属于金属元素;
故答案为:失去;金属;
(3)在同一周期中,从左到右各元素的原子最外层电子数逐渐增加;故答案为:在同一周期中,从左到右各元素的原子最外层电子数逐渐增加。
故答案为:增加。
(4)8号元素是氧元素,故组成的单质是氧气,一定条件下,2.4gCH4与8.0g O2恰好完全反应,5.4gH2O、2.2gCO2和物质X.则X的质量=2.4g+8.0g﹣5.4g﹣2.2g=2.8g;2.4gCH4中含有碳元素的质量为:2.4g×![]() =1.8g,故含有氢元素的质量为:2.4g﹣1.8g=0.6g;5.4gH2O中含有氢元素的质量为:5.4g×
=1.8g,故含有氢元素的质量为:2.4g﹣1.8g=0.6g;5.4gH2O中含有氢元素的质量为:5.4g×![]() =0.6g;2.2gCO2中含有碳元素的质量为:2.2g×
=0.6g;2.2gCO2中含有碳元素的质量为:2.2g×![]() =0.6g,故X中含有1.8g﹣0.6g=1.2g的碳,不含有氢元素,含有氧元素的质量为:8.0g﹣(5.4g﹣0.6g)﹣(2.2g﹣0.6g)=1.6g,故X中碳原子和氧原子的原子个数比为:
=0.6g,故X中含有1.8g﹣0.6g=1.2g的碳,不含有氢元素,含有氧元素的质量为:8.0g﹣(5.4g﹣0.6g)﹣(2.2g﹣0.6g)=1.6g,故X中碳原子和氧原子的原子个数比为:![]() :
:![]() =1:1.故该物质是一氧化碳;故填:CO;
=1:1.故该物质是一氧化碳;故填:CO;
(5)将镁、钙、铁、铜四种等质量的金属投入到足量的稀硫酸中,只有镁和铁与稀盐酸反应,反应速度最快的是镁,产生氢气最多的是镁。故填:镁;镁。