题目内容
【题目】以硫铁矿烧渣(主要成分Fe2O3、FeO、SiO2)为原料,制备高纯度氧化铁(Fe2O3)的生产流程示意图如图,回答下列问题。
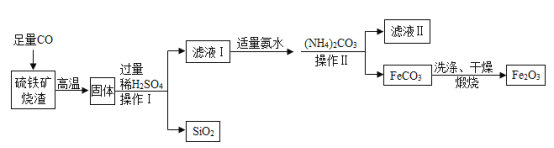
(1)操作Ⅰ、操作Ⅱ的名称是_____;
(2)写出高温时CO与硫铁矿烧渣反应生成Fe的其中一个化学方程式_____;
(3)写出加入过量稀硫酸发生反应的化学方程式_____;
(4)滤液Ⅰ的溶质是_____(填化学式)。
【答案】过滤 3CO+Fe2O3 2Fe+3CO2(或CO+FeO
2Fe+3CO2(或CO+FeO Fe+CO2) Fe+H2SO4=FeSO4+H2↑ FeSO4、H2SO4
Fe+CO2) Fe+H2SO4=FeSO4+H2↑ FeSO4、H2SO4
【解析】
(1)操作Ⅰ、操作Ⅱ都是得到固体和液体,为过滤。故填:过滤;
(2)硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2),所以高温时CO与硫铁矿烧渣反应生成Fe分别为氧化铁和一氧化碳或者氧化亚铁和一氧化碳在高温下生成铁和二氧化碳,对应的化学方程式Fe2O3+3CO  2Fe+3CO2或FeO+CO
2Fe+3CO2或FeO+CO Fe+CO2。故填:3CO+Fe2O3
Fe+CO2。故填:3CO+Fe2O3 2Fe+3CO2(或CO+FeO
2Fe+3CO2(或CO+FeO Fe+CO2);
Fe+CO2);
(3)过量的稀硫酸与生成的铁反应生成硫酸亚铁和氢气,反应的方程式为:Fe+H2SO4=FeSO4+H2↑,故填:Fe+H2SO4=FeSO4+H2↑;
(4)固体主要成分为铁,而加入过量硫酸,所以滤液I的溶质是生成的 FeSO4和剩余的H2SO4。故填:FeSO4、H2SO4。

【题目】有人提出使用“高科技的添加剂”可以使水变成汽油。小明同学在学习了“物质构成的奥秘”后,认为可以用物质组成的观点来驳斥这种说法。请回答问题。
(提出问题)根据水的组成和汽油的组成判断,水是否可以变成汽油?
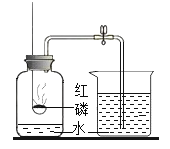
(猜想与验证)(1)确定水的组成。实验装置如图所示,该装置内反应的化学方程式为_________。实验一段时间后,检验a、b两管内收集的气体,其中b管内的气体可使_________(填现象),说明是__________。
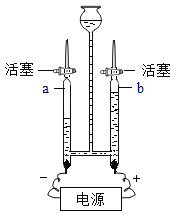
(实验结论)水是由氢元素和氧元素组成的。
(2)确定汽油的组成。操作如下:
实验步骤 | 实验现象 | 结论 |
①点燃汽油作燃料的灯;②将光洁干冷的烧杯罩在油灯火焰上方。 | 烧杯内壁产生雾状小液滴 | 证明汽油在空气中燃烧后的产物中有水。 |
③将内壁蘸有_______的烧杯罩在油灯火焰上方 | ________ | 证明汽油在空气中燃烧后的产物中有二氧化碳. |
(实验结论)汽油的组成中_____________。汽油和水的组成元素不同,水不能变成汽油。