题目内容
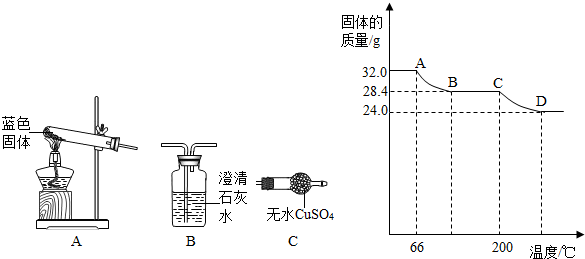
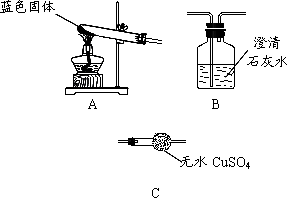
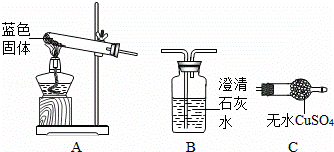
已知A、B、C三种固体含有同种金属元素,A难溶于水,B是一种氧化物,可作干燥剂.D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体.它们的转化关系如下图(部分产物已略去).(信息:X+2H2O=Ca(OH)2+C2H2↑)
(1)写出X物质的化学式:______.
(2)写出C→A的化学方程式:______.
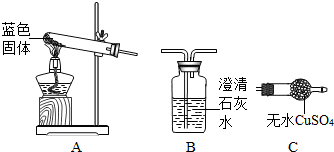
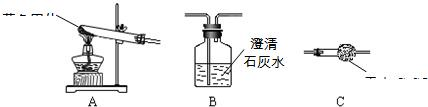
(3)实验室若分离由D和F组成的混合气体,如采用上图装置,则a中应盛有______(填写试剂名称,下同),b中应盛有______.
解:(1)在化学反应前后的原子个数不变,X+2H2O═Ca(OH)2+C2H2↑,故答案为:CaC2
(2)A难溶于水,会生成二氧化碳,所以A就是碳酸钙,A、B、C三种固体含有同种金属元素,B是一种氧化物,可作干燥剂,所以B就是氧化钙,X会转化成C,所以C就是氢氧化钙,
故答案为:Ca(OH)2+CO2═CaCO3↓+H2O
(3)二氧化碳是酸性氧化物会与碱反应,可以先将二氧化碳吸收,分出一氧化碳,然后再利用试剂分离出二氧化碳,吸收二氧化碳常用氢氧化钠,分离二氧化碳不能用盐酸,会引入氯化氢气体,故答案为:浓氢氧化钠溶液 稀硫酸
故答案为:(1)CaC2
(2)(OH)2+CO2═CaCO3↓+H2O
(3)浓氢氧化钠溶液 稀硫酸
分析:(1)根据质量守恒定律和X+2H2O═Ca(OH)2+C2H2↑,可知X就是CaC2,
(2)乙烯会转化成D,D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体,所以D就是二氧化碳,E是碳,F就是一氧化碳,A难溶于水,会生成二氧化碳,所以A就是碳酸钙,A、B、C三种固体含有同种金属元素,B是一种氧化物,可作干燥剂,所以B就是氧化钙,X会转化成C,所以C就是氢氧化钙,
(3)根据D、F的化学性质进行分析.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.
注意分离物质时,要根据物质的性质选择试剂,不能引入新的杂质.
(2)A难溶于水,会生成二氧化碳,所以A就是碳酸钙,A、B、C三种固体含有同种金属元素,B是一种氧化物,可作干燥剂,所以B就是氧化钙,X会转化成C,所以C就是氢氧化钙,
故答案为:Ca(OH)2+CO2═CaCO3↓+H2O
(3)二氧化碳是酸性氧化物会与碱反应,可以先将二氧化碳吸收,分出一氧化碳,然后再利用试剂分离出二氧化碳,吸收二氧化碳常用氢氧化钠,分离二氧化碳不能用盐酸,会引入氯化氢气体,故答案为:浓氢氧化钠溶液 稀硫酸
故答案为:(1)CaC2
(2)(OH)2+CO2═CaCO3↓+H2O
(3)浓氢氧化钠溶液 稀硫酸
分析:(1)根据质量守恒定律和X+2H2O═Ca(OH)2+C2H2↑,可知X就是CaC2,
(2)乙烯会转化成D,D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体,所以D就是二氧化碳,E是碳,F就是一氧化碳,A难溶于水,会生成二氧化碳,所以A就是碳酸钙,A、B、C三种固体含有同种金属元素,B是一种氧化物,可作干燥剂,所以B就是氧化钙,X会转化成C,所以C就是氢氧化钙,
(3)根据D、F的化学性质进行分析.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.
注意分离物质时,要根据物质的性质选择试剂,不能引入新的杂质.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
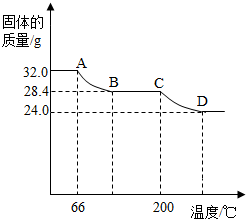
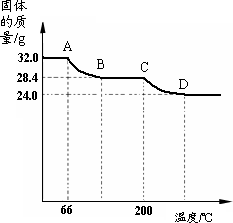
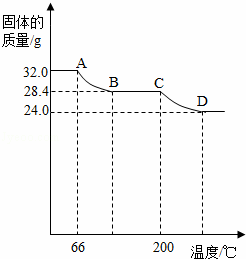
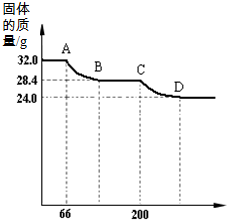 绘成固体质量变化与分解温度的关系如图,
绘成固体质量变化与分解温度的关系如图,