题目内容
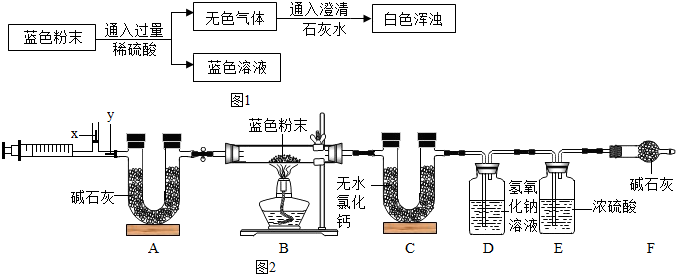
将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体.某研究性学习小组对蓝色固体的成分进行了如下探究.请完成下列各题:(一)猜想与假设:
猜想一:固体为CuCO3,理由:
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈
猜想三:固体为Cu(OH)2和CuCO3的混合物.
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物.
③无水硫酸铜遇水变蓝色.
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经过滤、洗涤、低温烘干得蓝色固体.
(2)判断固体已洗净的方法及现象
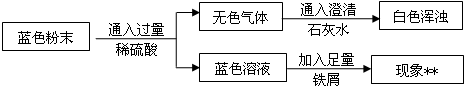
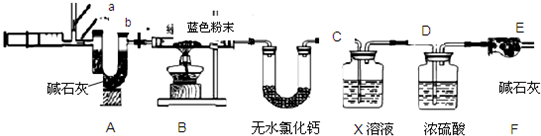
Ⅱ.用下图所示装置,定性探究固体的成分.
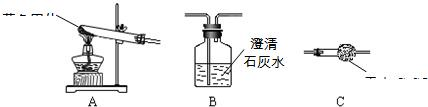
(3)若用装置A、B组合进行实验,B中无现象,则猜想
(4)若用装置A、C组合进行实验,C中无现象,则猜想
(5)小组同学将装置按 A、
结论:固体为Cu(OH)2和CuCO3的混合物.
Ⅲ.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃.设固体的组成为aCu(OH)2?bCuCO3.小组同学用热
分析仪对固体进行热分解,获得相关数据,
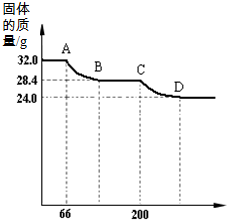 绘成固体质量变化与分解温度的关系如图,
绘成固体质量变化与分解温度的关系如图,请根据图示回答下列问题:
(6)写出A B、C D段发生反应的化学方程式:
AB段:
CD段:
(7)通过计算可得:a:b=
分析:(一)猜想与假设:①根据复分解反应的原理进行分析,
②根据碳酸钠在水中水解的产物进行分析.
(三)设计与实验:
(2)根据碳酸钠会与盐酸反应生成二氧化碳进行分析,
(3)根据氢氧化钙会与二氧化碳反应生成碳酸钙沉淀进行分析,
(4)根据无水硫酸铜遇水变蓝进行分析,
(5)根据检验水要放在检验二氧化碳的前面进行分析,
(6)根据氢氧化铜和碳酸铜的分解温度进行分析,
(7)根据氢氧化铜和碳酸铜分解的化学方程式进行分析.
②根据碳酸钠在水中水解的产物进行分析.
(三)设计与实验:
(2)根据碳酸钠会与盐酸反应生成二氧化碳进行分析,
(3)根据氢氧化钙会与二氧化碳反应生成碳酸钙沉淀进行分析,
(4)根据无水硫酸铜遇水变蓝进行分析,
(5)根据检验水要放在检验二氧化碳的前面进行分析,
(6)根据氢氧化铜和碳酸铜的分解温度进行分析,
(7)根据氢氧化铜和碳酸铜分解的化学方程式进行分析.
解答:解:(一)猜想与假设:
①碳酸钠和硫酸铜反应生成碳酸铜沉淀和硫酸钠,故答案为:Na2CO3+CuSO4=CuCO3↓+Na2SO4;
②碳酸钠是强碱弱酸盐,在水中水解后会生成氢氧根离子,故答案为:碱性
(三)设计与实验:
(2)固体上残留的碳酸钠会与盐酸反应生成二氧化碳气体,故答案为:取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3)B中无现象,说明没有生成二氧化碳,也就说明固体中没有碳酸铜,故答案为:二
(4)C中没有现象,说明没有水生成,也就说明固体中没有氢氧化铜沉淀,故答案为:一
(5)检验水要放在检验二氧化碳的前面,否则通过石灰水时携带的水蒸气会对检验水产生干扰,故答案为:A、C、B
(6)AB段的温度大于60℃但是没有超过200℃,从图象中看出也不超过100℃,符合氢氧化铁的分解温度,故答案为:Cu(OH)2
CuO+H2O;
CD段的温度超过了200℃,符合碳酸铜的分解温度,故答案为:CuCO3
CuO+CO2↑
(7)AB段是氢氧化铜在分解,固体质量减少3.6克,CD段是碳酸铜在分解,固体质量减少4.4克,
Cu(OH)2
CuO+H2O CuCO3
CuO+CO2↑
从方程式可以看出一个氢氧化铜分解会生成一个水,一个碳酸铜分解会产生一个二氧化碳,而AB段的氢氧化铜减少了3.6克水,减少了0.2个的水,需要0.2个氢氧化铜,CD段的碳酸铜分解减少了4.4克二氧化碳,相当于减少了0.1个二氧化碳,需要0.1个碳酸铜,所以a:b=2:1,故答案为:a:b=2:1
故答案为:(一)①Na2CO3+CuSO4=CuCO3↓+Na2SO4;
②:碱性
(三)(2):取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3):二
(4)一
(5)A、C、B
(6)Cu(OH)2
CuO+H2O;
CuCO3
CuO+CO2↑
(7)2:1
①碳酸钠和硫酸铜反应生成碳酸铜沉淀和硫酸钠,故答案为:Na2CO3+CuSO4=CuCO3↓+Na2SO4;
②碳酸钠是强碱弱酸盐,在水中水解后会生成氢氧根离子,故答案为:碱性
(三)设计与实验:
(2)固体上残留的碳酸钠会与盐酸反应生成二氧化碳气体,故答案为:取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3)B中无现象,说明没有生成二氧化碳,也就说明固体中没有碳酸铜,故答案为:二
(4)C中没有现象,说明没有水生成,也就说明固体中没有氢氧化铜沉淀,故答案为:一
(5)检验水要放在检验二氧化碳的前面,否则通过石灰水时携带的水蒸气会对检验水产生干扰,故答案为:A、C、B
(6)AB段的温度大于60℃但是没有超过200℃,从图象中看出也不超过100℃,符合氢氧化铁的分解温度,故答案为:Cu(OH)2
| ||
CD段的温度超过了200℃,符合碳酸铜的分解温度,故答案为:CuCO3
| ||
(7)AB段是氢氧化铜在分解,固体质量减少3.6克,CD段是碳酸铜在分解,固体质量减少4.4克,
Cu(OH)2
| ||
| ||
从方程式可以看出一个氢氧化铜分解会生成一个水,一个碳酸铜分解会产生一个二氧化碳,而AB段的氢氧化铜减少了3.6克水,减少了0.2个的水,需要0.2个氢氧化铜,CD段的碳酸铜分解减少了4.4克二氧化碳,相当于减少了0.1个二氧化碳,需要0.1个碳酸铜,所以a:b=2:1,故答案为:a:b=2:1
故答案为:(一)①Na2CO3+CuSO4=CuCO3↓+Na2SO4;
②:碱性
(三)(2):取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3):二
(4)一
(5)A、C、B
(6)Cu(OH)2
| ||
CuCO3
| ||
(7)2:1
点评:在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答,此类题难度较大,要细心进行分析解答.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案
相关题目