题目内容
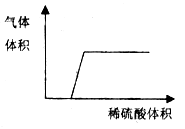
【题目】用氯酸钾和二氧化锰的混合物制取氧气,混合物的质量变化如右图,下列分析不正确的是( )
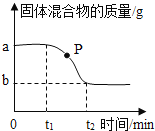
A. 反应结束时最多能收集到(a-b)g氧气
B. P点处固体成分是氯酸钾和氯化钾
C. 在反应过程中氯元素的质量分数不断增大
D. 在0~t2时段,MnO2在混合物中的质量不断增多
【答案】C
【解析】
氯酸钾在二氧化锰催化作用下生成氯化钾和氧气。
A、理论上反应结束时最多能收集到(a-b)g氧气,但是由于氧气可能有部分溶于水或部分氧气留在试管中,因此实际上收集的氧气会偏小,故A不正确;
B、P点处固体成分是氯酸钾部分分解生成的氯化钾,还有作为催化剂的二氧化锰,故B不正确;
C、在反应过程中,固体质量逐渐减少,而氯元素的质量不变,则氯元素的质量分数不断增大,故C正确;
D、在0~t2时段,MnO2在反应前后质量没变,混合物中的质量不变,故D不正确。故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】取10g锌粉和铜粉的混合物于烧杯中,向烧杯中分四次加入等质量的同种稀硫酸,实验过程中得到如下数据。
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸的质量 | 20g | 20g | 20g | 20g |
剩余固体的质量 | 8.7g | 7.4g | 6.1g | 5.5g |
(1)混合物中铜粉的质量是________。
(2)所用稀硫酸中溶质的质量分数是_____。(保留计算过程)