题目内容
【题目】请按题目要求回答:
(1)在CuCl2和FeCl2的混合溶液中加入一定质量的Mg粉,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀HCl,有气泡产生,则滤渣中一定含有的物质是_________________(填化学式)。
(2)某钢铁厂每天需消耗4900 t含Fe2O376%的赤铁矿石,该厂理论上可每天生产含Fe98%的生铁的质量是多少?(写出计算过程)____
【答案】Fe 2660t
【解析】
(1)在CuCl2和FeCl2的混合溶液中加入一定质量的Mg粉,镁粉先与铜发生置换反应,然后再与铁发生置换反应,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀HCl,有气泡产生,说明滤渣中一定有铁,可能有镁,则滤渣中一定含有的物质是:Fe。
(2)解:该厂理论上可每天生产含Fe98%的生铁的质量是x。
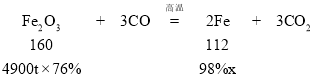
![]()
x=2660t
答:该厂理论上可每天生产含Fe98%的生铁的质量是2660t。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
【题目】将3份质量为8g的硫分别在一定量氧气中燃烧,记录数据如下表所示。
实验次数 | 第一次 | 第二次 | 第三次 |
氧气的质量 /g | 2 | 6 | 10 |
二氧化硫的质量 /g | 4 | 12 | 16 |
(1)该反应的化学反应方程式__________________;
(2)参加反应的硫、氧气和生成的二氧化硫之间的质量比为__________________;
(3)在第________次实验中,硫有剩余,剩余__________________ ;
(4)在第________次实验中,氧气有剩余,剩余__________________ g。