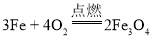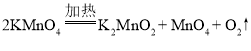题目内容
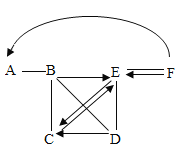
【题目】思维导图是激发大脑潜能,练就科学思维的有效方法。图中A、B、C、D、E、F分别表示初中化学常见的六种物质。B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前产量最大的金属,B由两种元素组成,C是大理石的主要成分。(图中用“一”表示两种物质之间能发生化学反应,用“→”或![]() 表示一种物质能转化为另一种物质, 部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。
表示一种物质能转化为另一种物质, 部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。
请回答下列问题。
(1)分别写出B、D物质的化学式: B_____,D_____。
(2)在E与F和F→A的反应中,F均表现出具有_____性。
(3)写出B与C发生反应的化学方程式_____。
(4)写出过量A的粉末与B发生反应的实验现象_____。
【答案】HCl Ca(OH)2 还原 ![]() 黑色粉末部分溶解,溶液由无色变成浅绿色,固体表面有气泡冒出
黑色粉末部分溶解,溶液由无色变成浅绿色,固体表面有气泡冒出
【解析】
A是目前产量最大的金属,则A为铁,C是大理石的主要成分,为碳酸钙,B、C、D、E分别为酸、碱、盐、氧化物类别中的一种,根据图中铁能与B反应,则B为酸,又因为B由两种元素组成,故B为稀盐酸,D能与酸反应,能与E反应,同时能转化为C,可推知D为氢氧化钙,能与氢氧化钙反应又能由稀盐酸反应制得,则E为二氧化碳,则F能与二氧化碳反应,也能转化为二氧化碳,同时能制得金属单质,则F为碳单质。
(1)由上分析知B为稀盐酸,化学式为:HCl,D为氢氧化钙,化学式为Ca(OH)2;
(2)E与F反应: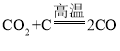 ,F到A的转化为:
,F到A的转化为: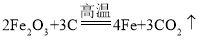 ;碳表现的均为还原性;
;碳表现的均为还原性;
(3)B为稀盐酸,C为碳酸钙,稀盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:![]() ;
;
(4)铁与稀盐酸反应生成氯化亚铁和氢气,故现象为黑色粉末部分溶解,溶液由无色变成浅绿色,固体表面有气泡冒出。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案【题目】利用金属活泼性的不同,可以采用不同的冶炼方法,请分析后作答:
冶炼方法 | 主要原理 | 代表金属 |
电解法 | 熔融的金属化合物在通电的条件下分解 | 钠、铝 |
热还原法 | 金属氧化物与一氧化碳(或碳等)在高温的条件下反应 | 铁、铜 |
热分解法 | 金属氧化物在加热的条件下分解 | 汞、银 |
(1)炼铁的原理是利用一氧化碳与氧化铁的反应,写出该反应的化学方程式:_____。
(2)从含有铅元素并有开采价值的矿石中提炼铅,应选择上述方法中的_____。
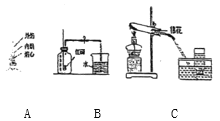
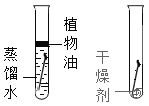
【题目】对比实验室实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
选项 | A | B | C | D |
实验设计 |
|
|
|
|
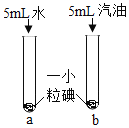
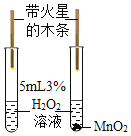
实验目的 | 探究CO2 与水发生了反应 | 探究水对铁钉锈蚀的影响 | 探究溶剂种类对物质溶解性的影响 | 探究MnO2是H2O2分解的催化剂 |
A.AB.BC.CD.D