题目内容
【题目】李阿姨很喜欢在网上淘宝,昨天她在网上买了一枚金戒指,比市场的价格要便宜很多,她既高兴又担心戒指是假的。于是她邀请你所在的化学兴趣小组的同学帮她测定戒指的真假。 查阅资料可知:假金(俗称黄铜,单纯从颜色、外形上看,与黄金极为相似,所以很难区分)是Zn、Cu合金,真金是Au(不考虑黄铜中的其他杂质)在托盘天平上称量这枚金戒指正好15g,将该金戒指放人烧杯中,用量筒量取75 mL稀盐酸分五次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀盐酸的体积/mL | 15 | 15 | 15 | 15 | 15 |
生成氢气的质量/g | 0. 04 | 0. 04 | 0. 04 | N | 0. 02 |
试求:
(1)由表中的数据我们可知:该金戒指为________(填“真”或“假”)
(2)N的数值为________。
(3)此金戒指中铜的质量分数是多少?_________(写出计算过程)
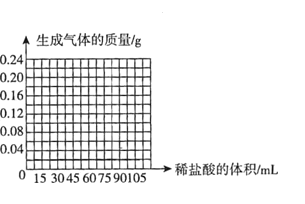
(4)请在下图中画出向这枚15g金戒指中加稀盐酸的体积与产生气体质量变化关系的示意图。______
【答案】假 0. 04 61% 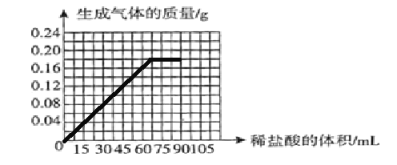
【解析】
(1)在金属活动性顺序表中,金在氢的后边,金不能与酸反应生成氢气,由表中的数据我们可知:该金戒指为假的;
(2)根据表格可以发现,第一、二、三次分别加入15mL盐酸,均生成0.04g氢气,第五次加入15mL盐酸还能生成并且只生成0.02g氢气,说明直到第五次反应才结束,并且盐酸有剩余;同时说明第四次加入15mL盐酸时完全反应,生成氢气的质量可按照第一次的数量关系(15ml对应0.04g)类推,而得出m为0.04g
(3)设此金戒指中锌的质量是x

![]()
x=5.85g
此金戒指中铜的质量分数是:
![]()
(4)由题中信息可知,每15mL盐酸时完全反应,生成氢气的质量0.04g,最后一次生成氢气0.02g,最后一次的盐酸反应掉一半,最终生成氢气共0.18g,在下图中画出向这枚15g金戒指中加稀盐酸的体积与产生气体质量变化关系的示意图。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案