题目内容
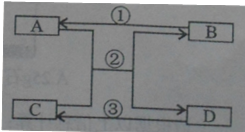
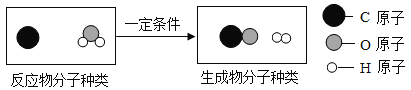
【题目】一定条件下,A和B反应生成C和D。反应前后分子种类变化的微观示意图如下所示:
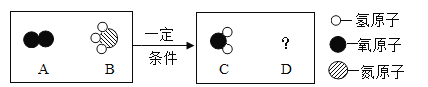
(1)A.B.C中属于单质的是_______(填字母);若B物质中氢元素的化合价为+1,则氮元素的化合价为__________;
(2)若D为空气中体积分数最大的气体,则该反应中生成的C和D的质量比为_______;
(3)若D为氧化物,且A和B的分子个数比为5: 4,则该反应的化学方程式为_______;
【答案】A -3 27:14 
【解析】
(1)A、B、C中只有A是氧气,由同一种元素组成的纯净物,属于单质,故填A;
B物质为NH3,若氢元素的化合价为+1价,设氮元素的化合价为x,根据化合物中,正负化合价的代数和为零,则x+3=0,x=-3,则氮元素的化合价为-3价;
(2)D为空气中体积分数最大的气体,则D为N2,则该反应的化学方程式为: ,则C和D的质量比为:(18×6):(14×4)=27:14;
,则C和D的质量比为:(18×6):(14×4)=27:14;
(3)D为氧化物,则D由氮元素和氧元素组成,A和B的分子个数比为5:4,根据质量守恒定律,化学反应前后元素的种类和数目不变,则D为NO,该反应的化学方程式为:

 名校课堂系列答案
名校课堂系列答案【题目】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的图象如图表所示:
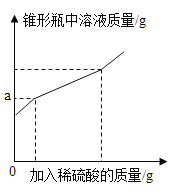
加入稀硫酸的质量/g | 40 | 65 | 75 |
产生气体的质量/g | 1.1 | 2.2 | 2.2 |
(1)6.5g样品与稀硫酸完全反应产生气体的质量是__________g。
(2)6.5g样品中碳酸钠的质量分数是___________。(结果精确至0.1%)
【题目】常温下,H2O2分解生成O2的速率较为缓慢。研究性学习小组选择“H2O2分解生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
(提出假设)催化剂的种类会影响H2O2分解生成O2的快慢。
(供选择的试剂)5%H2O2溶液、15%H2O2溶液、30%H2O2溶液、二氧化锰粉末、二氧化锰颗粒、氧化铜粉末
(设计方案)常温下,取两份5%H2O2溶液各100mL,分别加入_________,测量各生成一瓶相同O2所需的时间。
(实验探究)如图是他们进行实验的装置图,此实验中A处宜采用的气体收集方法是______。检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气体。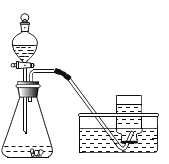
(实验记录)
实验编号 | ① | ② |
反应物 | 5%H2O2溶液100mL | 5%H2O2溶液100mL |
加入固体 | CuO | MnO2 |
收集一瓶气体所需时间 | 165s | 46s |
(实验分析)(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的___和___没有改变。
(2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以_________。
(得出结论)该探究过程得出的结论是____________,故实验室用H2O2溶液制取氧气的化学方程式为________。
(反思)还有哪些因素可能影响该反应的速率呢?
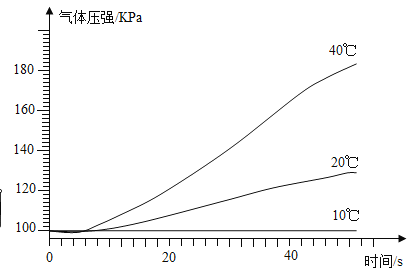
(1)在老师的帮助下,小组同学们使用压强传感器气体压强等设备,探究在其他条件相同时,不同温度下过氧化氢溶液分解时密闭容器内压强的变化。经过实验数据处理等,获得如图所示的压强-时间的曲线变化图。由此得出的结论是___________。
(2)你还有其他的猜想吗?
猜想:_____________。
请选择题目中提供的试剂,设计实验证明你的猜想(包括实验方案和结论)_____________。