题目内容
【题目】C919作为中国首款按照国际适航标准,并具备自主知识产权的民用飞机,是中国商飞在国际航空领域的鼎力之作。
(1)飞机材料往往使用大量的硬铝而不使用纯铝,硬铝属于_____(填“纯净物”或“混合物”),硬铝与纯铝相比,其熔点更_____填“高”或“低”),硬度更大。
(2)铁是飞机中常用的材料。在日常生活中,铁容易与_____(填化学式)发生化学反应而生锈,铁锈还可以“回炉”重新冶炼成铁,写出工业炼铁的原理_____(用化学方程式表示)。
(3)若要验证飞机材料中的铁、铝、铜金属的活动性顺序,只需一种试剂直接与上述三种金属反应就能达到目的,应选择的盐是_____(填化学式)。
【答案】混合物 低 O2、H2O 3CO+Fe2O3![]() 2Fe+3CO2 FeSO4
2Fe+3CO2 FeSO4
【解析】
金属生锈条件有氧气和水参与,铝与硫酸亚铁溶液反应生成硫酸铝溶液和铁。
(1)硬铝属于铝合金,属于混合物;硬铝与纯铝相比,其熔点更低,硬度更大。
(2)在日常生活中,铁容易与O2、H2O生锈,铁锈的主要成分是氧化铁,在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为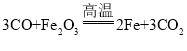 。
。
(3)在验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应,因此可选用硫酸亚铁(或氯化亚铁或硝酸亚铁)溶液,铝与硫酸亚铁溶液反应生成硫酸铝溶液和铁,铜不与硫酸亚铁溶液反应,可验证飞机材料中的Fe、Cu和Al的金属活动性顺序,故填:![]()

【题目】某化学小组在探究碱的化学性质时,做了如图所示的两个实验。
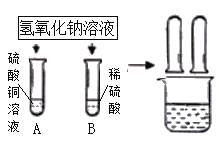
(1)写出A试管中发生反应的化学方程式________。
(2)实验结束后,同学们将A、B两试管中的废液倒入同一洁净的烧杯,烧杯中出现蓝色沉淀.小组同学将烧杯中的物质进行了过滤,对滤液中成分有如下猜想:
(提出猜想)甲:滤液中的溶质是Na2SO4
乙:滤液中的溶质是Na2SO4 、 H2SO4
丙:滤液中的溶质是Na2SO4 、 CuSO4
丁:滤液中的溶质是______
(交流讨论)同学们对以上的猜想提出质疑,认为猜想______不合理,理由是______
(设计实验)同学们通过以下的实验对猜想进行验证,请你完成实验报告。
实验内容 | 预计现象 | 预计结论 |
①取少量滤液于试管中,观察 | 溶液呈无色 | 猜想_____不成立 |
②继续在上述试管中加入______ | ______ | 猜想丁成立 |
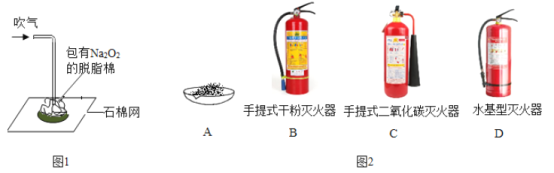
【题目】在化学学科节上,化学老师表演了“吹气生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上用吸管吹气,脱脂棉燃烧起来了(如图1)。同学们对实验产生了浓厚的兴趣。
(1)根据燃烧条件,脱脂棉是可燃物,小新认为过氧化钠(Na2O2)与吹出的CO2及H2O反应生成了可以支持燃烧的物质:而且还_____(填“吸收”或“放出”)热量,满足了燃烧的另一个条件_____。
(2)兴趣小组的同学将反应后的固体放入水中,发现固体全部溶解形成无色溶液,于是,对溶液中溶质成分进行探究。
(查阅资料)Na2O2是淡黄色固体,易与二氧化碳反应,也易与水反应,分别生成碳酸钠和氢氧化钠,都放出氧气。
(提出猜想)猜想一:溶质是Na2CO3;猜想二:溶质是NaOH;猜想三:溶质是_____。
(实验与探究)
实验步骤 | 实验现象 | 实验结论 |
1.取少量溶液于试管中,向其中滴加几滴无色酚酞,振荡 | 溶液红色 | 猜想二成立 |
2.另取反应后溶液少许于试管中,向其中滴加稀盐酸 | _____ | 猜想二不成立 |
3.取步骤1的溶液于试管中,向其中滴加足量的_____溶液,振荡 | ①_____②_____ | 猜想一不成立 |
(拓展与交流)
(1)小郑同学认为步骤1的实验结论不正确,请解释原因:_____。
(2)步骤2的实验现象说明有碳酸钠的存在,反应的化学方程式为_____。
(3)Na2O2也能与稀盐酸反应,生成氯化钠、水和氧气,反应的化学方程式为_____。
(4)化工厂存有过氧化钠,一旦失火不能选用图2中的灭火器材是_____(填字母)。