题目内容
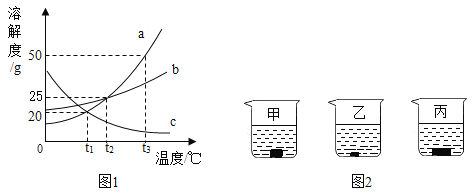
【题目】甲、乙、丙三种物质的溶解度曲线,如图所示,回答下列问题:
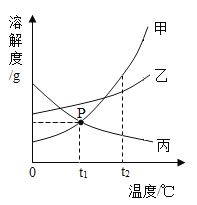
(1)P 点的含义____________________;
(2)t2℃时,甲、乙、丙三种物质溶解度从大到小的顺序为________________;
(3)当乙中混有少量甲时,可采用提纯乙的方法是________________(填“降温结晶”或“蒸发结晶”);
(4)t2℃时,将甲、乙、丙三种物质的饱和溶液同时降温t1℃,所得溶液中溶质质量分数由大到小的顺序为_______;
(5)配置一定溶质质量分数的乙溶液,可能导致所配溶液溶质质量分数偏大的是_____。
A.量取水的体积时俯视读数
B.所取固体中含有杂质
C.配制好的溶液,向细口瓶转移时溅出
D.称量完毕后,向烧杯内转移固体时纸上有乙残留
【答案】t1℃甲和丙的溶解度相等 甲>乙>丙 蒸发结晶 乙>甲>丙 A
【解析】
(1)通过分析溶解度曲线可知,P点的含义是:t1℃时,甲、丙物质的溶解度相等;
(2)t2℃时,甲、乙、丙三种物质溶解度从大到小的顺序为:甲>乙>丙;
(3)乙物质的溶解度受温度变化影响较小,所以当乙中混有少量甲时,可采用蒸发结晶的方法提纯乙;
(4)t1℃时,乙物质的溶解度最大,甲、丙物质的溶解度相等,降低温度,甲、乙物质的溶解度减小,丙物质的溶解度增大,应该按照t2℃时的溶解度计算,所以t2℃时,将甲、乙、丙三种物质的饱和溶液同时降温t1℃,所得溶液中溶质质量分数由大到小的顺序为:乙>甲>丙;
(5)A、量取水的体积时俯视读数,读数偏大,实际量取水的体积偏小,使用所配溶液溶质的质量分数偏高,故正确;
B、所取固体中含有杂质,则实际乙的质量偏小,使用所配溶液溶质的质量分数偏小,故错误;
C、溶液具有均一性,配制完后将溶液转移至试剂瓶时洒出了一些,溶质的质量分数不变,故错误;
D、称量完毕后,向烧杯内转移固体时纸上有乙残留,导致溶解乙的质量偏小,使用所配溶液溶质的质量分数偏低,故错误。