题目内容
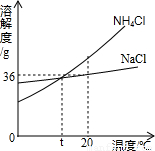
(2011?中山二模)根据如图判断,下列说法错误的是( )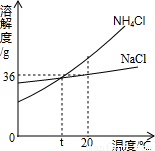
【答案】分析:根据固体的溶解度曲线可知:两物质的溶解度受温度变化的影响的情况;由溶解度可以确定能否形成饱和溶液、能判断饱和溶液溶质质量分数的大小.
解答:解:A、由图可知,NaCl和NH4Cl的溶解度都随温度升高而增大,故A正确;
B、20℃时,NaCl的溶解度为36g,故50克水中最多能溶解18克NaCl,故B正确;
C、t℃时,两物质的溶解度相等,故NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等,故C正确;
D、由于20℃时NH4Cl溶液可能是不饱和溶液,故降温到0℃,其溶质质量分数可能不变;
故选D.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,从而培养学生对固体溶解度的进一步的理解和应用.
解答:解:A、由图可知,NaCl和NH4Cl的溶解度都随温度升高而增大,故A正确;
B、20℃时,NaCl的溶解度为36g,故50克水中最多能溶解18克NaCl,故B正确;
C、t℃时,两物质的溶解度相等,故NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等,故C正确;
D、由于20℃时NH4Cl溶液可能是不饱和溶液,故降温到0℃,其溶质质量分数可能不变;
故选D.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,从而培养学生对固体溶解度的进一步的理解和应用.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
(2011?中山二模)某校兴趣小组在实验室中完成制取氧气的实验.他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为______g;
(2)根据表中数据分析M的值是______g
(3)原混合物中氯酸钾的质量分数是多少?(请写出计算过程)
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | M | 2.04 |
(1)完全反应后,生成氧气的质量为______g;
(2)根据表中数据分析M的值是______g
(3)原混合物中氯酸钾的质量分数是多少?(请写出计算过程)
 ”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:.
”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:.