题目内容
有3g混有碳酸钠的氯化钠固体样品,向其中滴加盐酸,加入盐酸的质量与生成二氧化碳气体的质量符合图所示的质量关系.(不计损耗)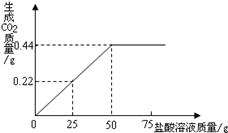
(1)样品完全反应后,共放出二氧化碳气体的物质的量为 mol。
(2)计算样品中氯化钠的质量分数。(根据化学方程式列式计算)
(1)0.01 (2)65%
解析试题分析:(1)有图像可知生成的二氧化碳的质量为0.44g,其物质的量为:0.44g/44g/mol=0.01mol
(2)设含碳酸钠xmol
Na2CO3+2HCl→2NaCl+CO2↑+H2O
1 1
X 0.01
1/x=1/0.01
X=0.01mol
m(Na2CO3)=0.01*106=1.06g
m(NaCl)=3-1.06=1.94g
氯化钠质量分数=1.94/3≈0.65=65%
答:氯化钠的质量分数为65%。
考点:物质量的计算、根据化学方程式的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。
| | 气体发生装置内物质的总质量 |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
(l)反应中二氧化锰的作用是 。
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。
 CaO+ CO2↑
CaO+ CO2↑