题目内容
(11分)红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。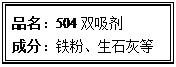
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示) 。
【实验探究1】
甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| ⑴取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液。 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有 ① 和氢氧化钙。 |
| ⑵另取少量固体放于试管中,滴加足量稀盐酸。 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有 ② , 一定不含Fe2O3。 |
| ⑶将步骤⑵中产生的气体通入到澄清的石灰水中。 | ③ | 固体中一定含有CaCO3。 |
⑴乙同学认为甲同学的实验中并不能得出一定含Ca(OH)2的结论,理由是
。
⑵丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是(用化学方程式表示) 、 。
【实验探究2】
乙、丙同学设计如下实验方案继续验证:
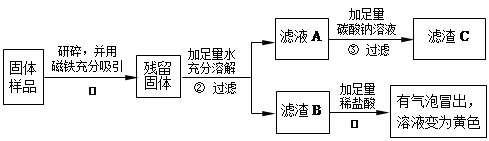
⑴ 乙、丙同学实验中又能得出固体样品中一定还含有 。
⑵ 乙同学经过实验测得上述滤渣C(CaCO3 )的质量为1.0 g,计算滤液A中含氢氧
化钙的质量。(写出解题过程)
⑶ 丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6 g,滤渣B中CaCO3的质量为1.0 g。
【实验结论】综合上述实验以及乙、丙两位同学的实验数据,久置固体的成分是:
【作出猜想】CaO + H2O ="==" Ca(OH)2
【实验探究1】①CaO ②Fe ③澄清的石灰水变浑浊
【实验质疑】(1)氧化钙与水反应生成的氢氧化钙也能使无色酚酞变红,不能确定原固体中是否含有氢氧化钙
(2)Fe2O3 + 6HCl = 2FeCl3 + 3H2O Fe + 2FeCl3 = 3FeCl2
【实验探究2】(1)Fe2O3 (2)0.74g
【实验结论】Fe、Fe2O3、CaO、Ca(OH)2、CaCO3
解析试题分析:【作出猜想】久置固体中可能含有Ca(OH)2的原因是:氧化钙会吸收水分反应生成Ca(OH)2,化学方程式表示:CaO + H2O ="==" Ca(OH)2
【实验探究1】①氧化钙与水分反应过程中会放出大量的热,所以根据固体溶解时试管外壁发烫的现象,所以固体中一定含CaO
②根据铁会与盐酸反应产生氢气和氯化亚铁,氯化亚铁是浅绿色溶液,故根据现象,可判断归中一定含铁
③因为实验结论固体中一定含有CaCO3,它会与盐酸反应产生二氧化碳,而二氧化碳能使澄清的石灰水变浑浊
【实验质疑】⑴乙同学认为甲同学的实验中并不能得出一定含Ca(OH)2的结论,理由是:氧化钙与水反应生成的氢氧化钙也能使无色酚酞变红,不能确定原固体中是否含有氢氧化钙
⑵丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是有可能是Fe2O3与盐酸反应生成氯化铁溶液,而铁与氯化铁溶液在常温下发生反应生成氯化亚铁,所以化学方程式:Fe2O3 + 6HCl = 2FeCl3 + 3H2O,Fe + 2FeCl3 = 3FeCl2
【实验探究2】⑴ 乙、丙同学实验中,在滤渣B中加入盐酸,溶液变为黄色,所以能得出固体样品中一定还含有Fe2O3
⑵根据化学反应:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH中CaCO3与Ca(OH)2的质量关系,即可求出滤液A中含氢氧化钙的质量
解:设滤液A中氢氧化钙的质量为X
Ca(OH)2+Na2CO3==CaCO3↓+2NaOH
74 100
x 1.0g
74:100=x:1.0g
∴x=0.74g
【实验结论】通过上面的计算滤液A中氢氧化钙的质量为0.74g,假设原固体中没有CaO,那么含钙的物质就两种:Ca(OH)2和CaCO3,但质量1.0g+0.74g>1.6g,说明0.74g的氢氧化钙应该来自两部分,一是氧化钙与水反应生成的,二是原有的,所以可以确定久置固体的成分是:Fe、Fe2O3、CaO、Ca(OH)2、CaCO3
考点:化学反应中的热现象,酸的化学性质,酸碱指示剂变色情况,根据化学方程式计算

(6分)在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是 ,白色物质可能是Na2O或Na2CO3或 ,乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是: 。
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠: Na2O+H2O ="=" 2NaOH
【实验探究】甲同学对白色物质进行实验探究。
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质 为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质 是 。 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【得出结论】钠在二氧化碳中燃烧的化学方程式为: 。
(6分)市售“管道通”能使堵塞的管道畅通。小华通过实验对“管道通”中的物质成分进行了探究。
提出问题:“管道通”中含有什么物质?
查阅资料:
(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道。
(3)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热。例如,铝与盐酸反应的化学方程式是: ,铝与氢氧化钠溶液反应的化学方程式是:2Al+2NaOH+ ═2NaAlO2+3H2↑
猜想与验证:小华打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末。
猜想Ⅰ:白色固体颗粒为氢氧化钠。实验方案如下表所示:
| 实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿 | |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 | |
| ③向操作②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
猜想Ⅱ:银灰色粉末为铝粉。
实验:取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加 溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色。
结论:银灰色粉末为铝粉。
交流与反思:(1)老师告诉小华,氢氧化钾和氢氧化钠的性质非常相似.因此,要确认猜想Ⅰ是否正确,还需要学习如何检验钠元素的存在.
(2)使用管道通时,先将其中银灰色粉末添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水后立即堵上管道口,管道内迅速发生反应.请写出一个使用“管道通”时的注意事项:
。
(7分)化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
【提供资料】① 二氧化碳与过氧化钠反应生成氧气和另一种物质。
②Na2O2是一种淡黄色固体,常温下能与H2O、HCl气体等物质发生反应,生成氧气不能与N2发生反应。
(1)探究二氧化碳与过氧化钠反应生成氧气。
同学们在老师的指导下设计了如下图所示装置。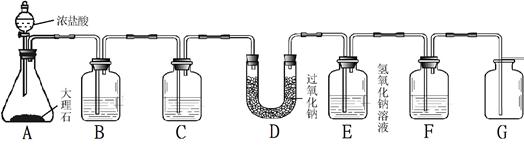
① 写出检验G中气体的方法 。
②若无装置C,对实验有影响的物质是 。
③若观察到 ,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
【猜想与假设】下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
你认为猜想 是不正确的,理由是 。
【进行实验】排除错误猜想后,同学们通过以下实验验证了另一种物质。
| 实验操作 | 实验现象 |
| 取少量CO2与Na2O2反应后的固体于试管中,加入稀盐酸。 | 有大量气泡产生 |
①某同学认为上述方案存在不足,他的理由是 。
②写出过氧化钠与二氧化碳反应的化学方程式 。
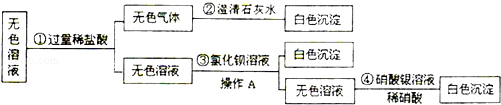
(8分)实验室中有一瓶标签受损的无色液体,如图所示。
这瓶无色液体是什么呢? 实验员老师告诉大家,该液体只能是硫酸钠溶液、
氯化钠溶液和蒸馏水中的一种。
(1)大家讨论后一致认为不可能是蒸馏水,理由是 。
(2)为确定该液体成分,同学们继续进行了如下实验探究,请完成实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| | 没有沉淀产生。 | 该液体不是硫酸钠溶液。 |
| | | 该液体是氯化钠溶液。 |
电池是日常必备用品之一,但它也是环境污染的一个重要来源。下面是某兴趣小组利用废旧锌锰干电池作为原料,并进行相关探究的过程。
【知识储备】
(1)锌锰电池的构造和组成(见图)。
(2)结晶水合物的特殊性质:在逐步升高温度条件下,
结晶水合物能失去部分或者全部结晶水,如蓝色的胆矾
晶体(CuSO4 ?5H2O)受热时可失去结晶水变为白色的无
水硫酸铜粉末(CuSO4)。
(Ⅰ)制备皓矾晶体(ZnSO4?xH2O)
小组同学参观了某回收废旧锌锰电池的工厂,其回收工艺流程如图: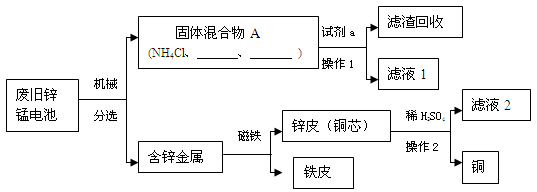
将滤液2蒸发浓缩、冷却结晶可得到皓矾晶体(ZnSO4?xH2O),蒸发时要用要用玻璃棒不断搅拌,目的是防止 引起液滴飞溅。
(Ⅱ)兴趣拓展——回收二氧化锰
实验(Ⅰ)中部分步骤可回收较纯净的二氧化锰固体。
 (1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。
(1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。
(2)在空气中充分灼烧的目的是 。
(Ⅲ)皓矾晶体中结晶水含量的测定
小组同学将部分皓矾晶体(ZnSO4?xH2O)带回实验室,用下图装置测定晶体中结晶水的含量(图中半透膜可让气体通过又可防止固体粉末进入导管)。
测定方法:称取28.7g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水:
(ZnSO4?xH2O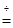 ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
(1)B中的试剂可从下列物质中选取,你的选择是 。
| A.浓硫酸 | B.硝酸银溶液 | C.饱和碳酸钠溶液 | D.澄清石灰水 |
(3)根据实验结果,计算皓矾晶体中结晶水的x值为 。
(9分)优质珍珠粉和廉价“珍珠粉”价格相差很大,但外观、手感没有明显差异,某化学兴趣小组同学对二者成分的不同进行了探究。
【查阅资料】
①优质珍珠粉由珍珠加工而成,含有一定量的碳酸钙、氨基酸等;氨基酸大部分能溶解于水,遇到浓硝酸并加热会呈现黄色或黑色。
②廉价“珍珠粉”由贝壳加工而成,加工过程中会用到氢氧化钠;贝壳的主要成分是碳酸钙。
③优质珍珠粉和廉价“珍珠粉”中,除碳酸钙外,其他成分均不能与盐酸反应生成二氧化碳。
【提出猜想】优质珍珠粉和廉价“珍珠粉”的区别可能有:
①廉价“珍珠粉”中含有 。
②廉价“珍珠粉”中不含氨基酸。
③优质珍珠粉和廉价“珍珠粉”中碳酸钙的质量分数不同。
【实验Ⅰ】将少量优质珍珠粉和廉价“珍珠粉”分别放入两只烧杯中,加少量水溶解,静置一段时间后过滤,取两种滤液备用。
| 操作 | 现象 | 结论 |
| 取少量两种滤液分别于两支试管中,滴加少量 | 优质珍珠粉的滤液没有变色;廉价“珍珠粉”的滤液变红 | 猜想①成立 |
| 取少量两种滤液分别于两支试管中,加入一定量 ,加热至沸腾 | 优质珍珠粉的滤液有黄色出现,局部变黑;廉价“珍珠粉”的滤液没有明显现象 | 猜想②成立 |
| | 优质珍珠粉 | 廉价“珍珠粉” |
| 固体粉末的质量 | 10.00 g | 10.00 g |
| 加入稀盐酸的质量 | 46.00 g | 50.13 g |
| 反应后烧杯中物质的质量 | 52.00 g | 55.77 g |
(请写出计算过程,结果保留至0.1%)
得出结论:廉价“珍珠粉”中碳酸钙的质量分数 优质珍珠粉(选填“高于”、“低于”或“等于”)。
【反思与评价】已知实验Ⅱ中所用稀盐酸的质量分数为14.6% 。小明提出:用加入稀盐酸的质量乘以其质量分数,求出参加反应的氯化氢的质量,进而利用化学方程式也能求出廉价“珍珠粉”中碳酸钙的质量。你认为小明的思路是否可行? (选填“可行”或“不可行”)。你的理由是 。
(8分)实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如右图所示)。实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中。
(1)甲同学的实验中向 中滴加石蕊试液后,溶液颜色为红色。
(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有 。
A.HCl B.NaOH C.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
,② ,③ 。
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
| 操作方法 | 实验现象 | 实验结论 |
| | | |
(4)最后,两位同学向烧杯C中加入 ,实现了此次实验的绿色排放(呈中性)。