题目内容
【题目】某金属冶炼场在生产过程中产生了一些含铜废料。化学兴趣小组利用稀硫酸和铁粉分离回收铜,并得到硫酸亚铁晶体。

(查阅资料)
(1)在同温同压下相同体积的气体含有的分子个数相同;
(2)在通入空气和加热的条件下,铜可以和稀硫酸反应生成硫酸铜,反应的化学方程式是2Cu +2H2SO4+ O2 ![]() 2CuSO4 + 2H2O 。
2CuSO4 + 2H2O 。
(回答问题)
(1)步骤I中分离得到固体A和蓝色溶液B的操作名称是_____;
(2)蓝色溶液B的溶质是_____(填化学式);
(3)写出反应Ⅲ中发生反应的化学方程式_____;
(4)铜制品可以在空气中发生锈蚀,铜锈化学式为Cu2(OH)2CO3,根据铜锈的化学式可以判断铜锈蚀需要空气中的_____(写化学式)。
(拓展研究)
小明通过查阅资料,利用铁粉、碳粉、氯化钠等物质进行了实验(如装置图),9分钟后测得数据如下表:

实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 量气管内液面所在刻度 | 量气管内液面所在刻度 |
150.0mL | 30.8mL | 0.2mL |
(1)请计算出空气中的氧气含量_____;
(2)碳粉和氯化钠在本实验中的作用是_____;
(3)若将装置中的粗铁粉换成足量的铜粉进行实验,请判断能否比较准确的测定出空气中氧气的体积分数,请说明理由_____。
【答案】过滤 CuSO4 Fe+H2SO4==FeSO4+H2↑ O2、H2O、CO2 20.4% 吸收水蒸气和氧气,腐蚀铁钉加速锈蚀(意思正确即可) 不能,因为铜锈蚀需要二氧化碳的参与,而瓶中的二氧化碳很少,难于让铜锈蚀
【解析】
(1)步骤I分离得到固体A和蓝色溶液B,固液分离,是过滤操作;
(2)由资料2可知,蓝色溶液为硫酸铜溶液,故溶质为硫酸铜(CuSO4);
(3)步骤三生成硫酸亚铁溶液和气体可知,该反应的化学方程式为Fe+H2SO4==FeSO4+H2↑;
(4)铜锈化学式为Cu2(OH)2CO3,结合质量守恒定律,可推知铜生锈是与空气中氧气、二氧化碳、水蒸气共同作用的结果;
【拓展研究】
(1)消耗氧气体积为:30.8mL-0.2mL=30.6mL,则空气中氧气含量为:![]() ;
;
(2)碳粉和氯化钠在本实验中的作用是吸收水蒸气和氧气,腐蚀铁钉加速锈蚀;
(3)不能,因为铜锈蚀需要二氧化碳的参与,而瓶中的二氧化碳很少,铜很难锈蚀,实验结果不准确。

【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)
I.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后_____。
(实验)用天平称量0.2gCuO,取5ml 5%的过氧化氢溶液于试管中,进行如下实验:
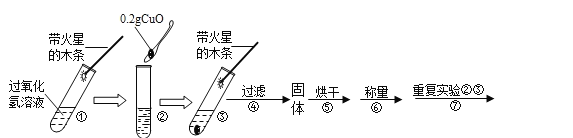
(1)填写下表:
步骤③的现象 | 步骤⑥的结果 | 步骤⑦的现象 | 结论 |
带火星的木条复燃 | _____ | _____ | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立 |
(2)步骤①的目的是_____,步骤⑦的目的是:_____。
(3)步骤⑥用到的主要实验仪器是_____。
(4)过氧化氢能被CuO催化分解放出O2反应的符号表达式_____。
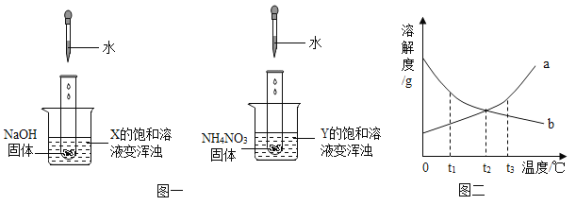
【题目】甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
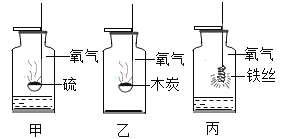
(1)所发生的三个反应有多个共同的特点,分别是:①________________, ②_________________,
(2)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是________,甲瓶中反应的文字表达式为______________。
(3)小明做完上述实验后,在乙中加入了一种无色液体,他所加的液体可能是________(填名称);加该液体的目的是 ______________
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。他将镁条和不同含碳量的铁丝(铁丝直径均为0.4 mm)放入氧气中燃烧,并将现象记录在下表中。
物质 | 镁 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,火星四射 |
①小明实验前将铁丝绕成螺旋状的目的是________。
②铁丝在氧气中燃烧的文字表达式 __________。