题目内容
【题目】下表是空气中的气体成分和人体呼出的气体成分含量对照表:
气体成分 | 氮气 | 氧气 | 二氧化碳 | 水 | 其他气体 |
空气(%) | 78 | 21 | 0.03 | 0.07 | 0.9 |
呼出的气体(%) | 78 | 16 | 4 | 1.1 | 0.9 |
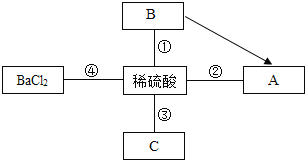
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入空气成分的含量有什么不同,其主要操作步骤如图所示.
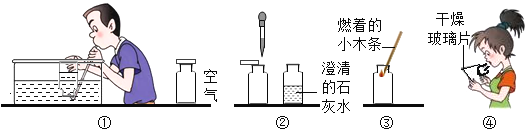
请依据图示将主要实验操作步骤及验证依据填入下表中:
实验步骤 | 验证依据 |
① | |
② | 根据_____ 判断二氧化碳含量不同 |
③ | 根据_____ 判断氧气含量不同 |
④ | 根据_____ 判断水含量不同 |
归纳总结:归纳总结也是学好化学的一种重要的方法,现请你概括总结你已知道的二氧化碳的性质:_____.
【答案】石灰水浑浊程度的不同 木条燃烧情况的不同 玻璃片上水雾的不同 二氧化碳是一种无色无味密度比空气大的气体,能溶于水,能与澄清石灰水发生反应
【解析】
利用氧气能助燃,能使燃着的木条燃烧更旺,二氧化碳能使澄清石灰水变浑浊,水蒸气遇冷变成液态的水,解决此题方案为:
实验步骤 | 验证依据 | ||
将澄清的石灰水分别滴入盛有呼出的气体和空气的集气瓶中 | 根据石灰水浑浊程度的不同判断CO2含量不同 | ||
将燃着的木条分别放入盛有呼出的气体和空气的集气瓶中 | 根据木条燃烧情况的不同判断O2含量不同 | ||
取两块干燥的玻璃片,对着其中的一块呼气 | 根据玻璃片上水雾的不同判断水含量不同 | ||
实验步骤 | 验证依据 | ||
石灰水浑浊程度的不同 | |||
木条燃烧情况的不同 | |||
玻璃片上水雾的不同 | |||

【题目】某兴趣小组的同学对实验室制备氧气的条件进行如下实验探究.
(1)小明同学知道二氧化锰能做过氧化氢分解的催化剂后,想再探究其它物质是否也可做过氧化氢分解的催化剂.请你一起参与他的探究过程,并填写下列空白:
(提出问题)氧化铜能否做过氧化氢分解的催化剂?如果能,其催化效果如何?
(设计并完成)
实验步骤 | 实验现象 |
I.分别量取 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象 |
II.持A试管中没有现象发生时,重新加入5%的过氧化氢溶液,并把带火星的木条伸入试管中,如此反复几次实验,观察现象. | 试管中均产生气泡,带火星的木条均复燃. |
III.将实验中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为 | |
IV.分别量取 |
(实验分析)
①实验II、III证明:氧化铜的________和________在反应前后均没有发生变化,________(填“能”或“不能”)作为过氧化氢分解的催化剂.
②实验设IV的目的是____________.
(2)小丽同学想探究二氧化锰的用量对过氧化氢分解速率的影响.她做了这样一组实验每次用![]() 的过氧化氢溶液,采用不同量的二氧化锰粉末做实验,测定各收集到
的过氧化氢溶液,采用不同量的二氧化锰粉末做实验,测定各收集到![]() 氧气时所用的时间,结果如下(其它实验条件均相同)
氧气时所用的时间,结果如下(其它实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
时间(秒) | 22 | 13 | 12 | 10 | 9 | 8 | 5 | 3 | 3 | 3 |
请分析表中数据,可以得出的结论是:____________.
(3)除是否使用催化剂、催化剂的种类、催化剂的质量外,还可能有哪些因素会影响过氧化氢的分解速率,你的猜想是________(任写一条即可).