题目内容
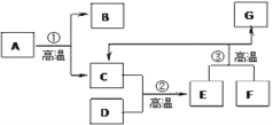
【题目】A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均已略去):
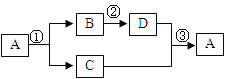
(1)写出①反应的化学方程式________________;
(2)D可能是______________(填化学式);
(3)C的一项用途是是____________________。
【答案】2H2O![]() 2H2↑+ O2↑ CuO; 冶炼金属。
2H2↑+ O2↑ CuO; 冶炼金属。
【解析】
(1)A、B、C、D都是初中化学中的常见物质,A是人类赖以生存的一种无色液体,所以A是水,水通电分解生成氢气和氧气,所以B和C是氢气和氧气中的一种,B能转化生成黑色固体D,且D能与C反应生成水,所以可能是发生的氢气还原金属氧化物的反应,所以C是氢气,B是氧气,D是氧化铜,经过验证,推导正确,所以①反应是水在通电的条件下生成氢气和氧气,化学方程式为:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
(2)D可能是CuO;
(3)C的一项用途是冶炼金属。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】同学们对H2O2溶液分解的反应速率的影响因素进行探究。
实验1:探究H2O2溶液浓度、温度对反应速率的影响
(实验方案)在一定温度下,向相同质量的H2O2溶液中加入相同质量的MnO2粉末,测量收集150 mL O2所需的时间。
实验序号 | H2O2溶液的浓度/% | 温度/℃ | 时间/s |
I | 30 | 20 | 待测 |
II | 15 | 30 | 待测 |
III | a | b | 待测 |
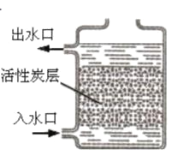
实验2:依据下图装置进行实验(部分仪器略去),探究催化剂种类对反应速率的影响
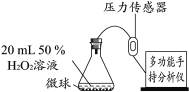
用相同粒数的MnO2、CuO、Fe2O3、Cr2O3四种催化剂微球(质量相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如下图。

(解释与结论)
(1)实验1中反应的化学方程式是______。若要制得3.2 gO2,需要H2O2的质量为______g。
(2)为了达到实验1的目的,补全实验方案。
① 若a与b不相等,则a=______;b=______。
② 若a与b相等,则设计实验I、III的目的是______。
(3)实验2中使用相同粒数催化剂微球的原因是______。
(4)通过对实验2数据的分析,可得出的结论是______。
(反思与评价)
(5)实验1是通过测量收集等体积O2所需时间来比较H2O2溶液的反应速率,还可以通过测量______来比较H2O2溶液的反应速率。
【题目】化学兴趣小组的同学通过查阅资料得知:过氧化氢分解除了二氧化锰作为催化剂,还可以用氧化铁、氧化铜等作为催化剂,于是他们开展了以下探究:
(探究(一))氧化铁能否做过氧化氢分解的催化剂?
项目 | 实验操作 | 实验现象 | 实验解释与结论 | |
解释 | 结论 | |||
实 验 一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是①_____ | 氧化铁是过氧化氢分解的催化剂 |
实 验 二 | 向盛有5mL5%过氧化氢溶液的试管中加入氧化铁,伸入带火星的木条 | ②_____ | 氧化铁能加快过氧化氢的分解 | |
(交流与反思)小岑同学认为仅由上述实验还不能得出表内的结论,他补充设计了两个方面的实验操作:第一方面的实验操作中包含了两次称量,其目的是探究反应前后氧化铁的③_____是否改变。第二方面的实验操作是利用“实验二”反应后试管内的固体剩余物继续实验,其目的是探究反应前后氧化铁的④_____是否改变。
(探究(二))为了探究不同的催化剂对过氧化氢的催化效率,兴趣小组继续设计并进行了如下实验:
实验装置 | 实验编号 | 实验药品 | 收集10mL氧气的时间(s) |
| 1 | 5mL5%的过氧化氢溶液,0.5g二氧化锰 | 30 |
2 | 5mL10%的过氧化氢溶液,0.5g氧化铁 | 60 | |
3 | 5mL10%的过氧化氢溶液,0.5g氧化铜 | 20 |
(交流与反思)
(1)探究(二)与探究(一)实验方法相同,均属于⑤
(2)写出实验1的反应的化学方程式⑥_____;
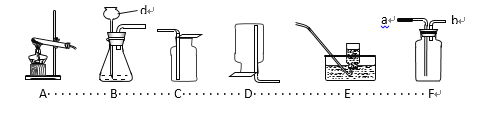
(3)如图实验装置的连接顺序依次为:a→⑦_____→⑧_____→d(填接口字母);
(4)小茜根据表中数据分析得出结论:三者中氧化铜的催化效率最高,但是小诗却认为该结论并不可靠,理由是⑨_____;同学们根据小诗的建议重新设计并进行了实验,得出了正确的结论。