题目内容
【题目】化学促进了人类社会的发展
(1)材料的应用和发展标志人类的进步,下列属于有机合成材料的是_____
A 陶瓷 B 青铜 C 聚乙烯 D 合成纤维
(2)下列事实与化学无关的是_____
A 发展低碳经济,保护环境 B 日环食、日偏食的产生
C 开发新能源,研制新材料 D 药物和保健品的研制
(3)食用盐中添加碘酸钾(KIO3)可有效预防甲亢,KIO3“I”的化合价为_____.
(4)氧化钙、铁粉、氯化钙均可作食品的干燥剂,其中,属于氧化物的是_____.
(5)测定地下水的酸碱度可用_____(填“紫色石蕊溶液、无色酚酞溶液 或pH试纸)在自来水消毒中的微观过程可用如图表示:
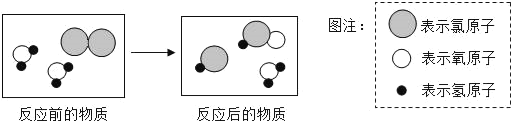
该反应的化学方程式为_____.
【答案】(1)C、D (2)B(3)+5(4)氧化钙
(5)pH试纸; H2O+Cl2→HCl+ HClO
【解析】
试题(1)聚乙烯、合成纤维都属于有机合成材料;
(2)ACD都是与化学有关的事项,日环食、日偏食的产生是星体运动的自然现象,跟化学无关;
(3)设,KIO3“I”的化合价为X。(+1)+X+(-2)×3=0,X=+5;
(4)氧化钙是由氧元素和钙元素两种元素组成的化合物,属于氧化物;
(5)测定地下水的酸碱度可用pH试纸;自来水消毒中的化学方程式为H2O+Cl2="HCl+" HClO 。

【题目】全世界每年因生锈而损失的钢铁约占世界钢铁年产量的1/4.某同学想探究铁生锈的条件,他将干净的铁钉分别同时放入A、B、C三支试管中进行探究。
(设计实验)请你帮助该同学完成下列实验设计的内容:
编号 | 操作方法 | 实验目的 |
A | 在干燥的试管中放入铁钉,并放入少量氯 化钙做干燥剂 | 探究铁在_____铁的生锈情况 |
B | 放入铁钉,注入蒸馏水浸没铁钉,并用植 物油液封 | 探究铁在_____铁的生锈情况 |
C | _____ | 探究铁在有氧气和水同时存在时的生锈情况 |
(实验结论)一周后,编号为_____的试管中的铁钉最易生锈。
(扩展延伸)苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样。
(1)切开的苹果“生锈”与什么因素有关?
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”。
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”。
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”。
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”。
(2)查阅资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质。且不切开的苹果没有此现象,所以苹果“生锈”与猜想①无关。
(3)在②﹣④猜想中,你认为猜想_____最不合理,理由是_____。
(实践应用)(1)用相同材料制作,经过相同防锈处理的铁栏杆,安装在沿海比安装在内陆更易生锈,其主要原因是_____。
(2)有时候铁制品腐蚀不一定是因为锈蚀而引起的,如用铁桶盛装农药波尔多液(含硫酸铜溶液)就很容易被腐蚀,写出该反应的化学方程式_____。
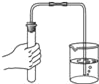
【题目】某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验,实验中观察到试管a内发生的现象是_____,试管b内澄清石灰水变浑浊,证明有_____生成.
实验在高温条件下充分反应.兴趣小组对实验后试管a内的固体成分发生了兴趣,激发了探究热情.
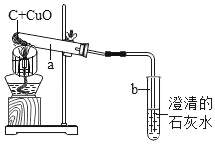
(提出问题):“反应后试管a内的固体物质是什么?
(进行猜想):小静同学认为该固体全部是铜;
小华同学认为该固体是铜与氧化铜两种物质的混合物;
小东同学认为该固体是铜与_____两种物质的混合物;
小明同学认为该固体可能是铜、木炭和氧化铜三种物质的混合物
小华认为因为是充分反应,所以_____同学的猜想明显不成立
(查阅资料)稀硫酸是无色液体:
木炭、铜都不与稀硫酸反应,氧化铜能与稀硫酸反应得到蓝色硫酸铜溶液
(实验设计)
实验操作 | 实验现象 | 实验结论 |
取少量固体物质于试管中,加足量稀硫酸充分震荡 | 黑色固体溶解,溶液变成蓝色 | 固体中有_____ |
(反思评价):_____同学的评价是正确的;
(定量探究):现取炭碳与氧化铜的混合物18g,高温条件下充分反应,剩余固体的质量为13.6g,经测定其中氧化铜有剩余,请通过计算确定原混合物中碳和氧化铜各有多少克_____?
【题目】南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如图1所示.南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究.
(提出问题)久置固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
(作出猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
(实验探究)
南南同学的方案:
实验操作 | 实验现象 | 实验结论 |
取少量固体放于试管中,滴加足量的_____. | 固体逐渐消失,有无色气体产生,得到浅绿色溶液. | 固体中一定含有_____, 一定不含Fe2O3. |
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是_____,并设计如图2实验方案继续验证.
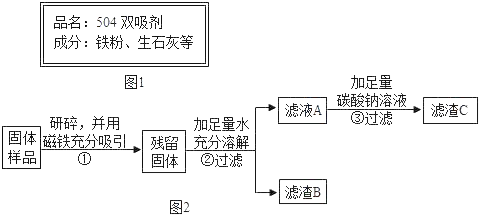
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是_____.
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有_____.写出该过程中的化学方程式_____.
(3)步骤③中反应的化学方程式是_____.
北北同学对滤渣B又进行探究.
实验操作 | 实验现象 | 实验结论 |
①取滤渣B于试管中,加入适量 _____ ②生成的气体通入_____ | ①固体减少,_____ ②该溶液变浑浊. | 固体中一定含有CaCO3 和Fe2O3. |
(实验结论)综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3.
(实验拓展)为增强双吸剂的吸收效果,常在双吸剂中加入一定量的NaCl,NaCl的作用可能是_____.
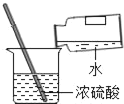
【题目】小明在学习金属活动性顺序后,知道钾、钙、钠的金属活动性特别强,能与水反应生成碱和氢气。他思考镁紧排在钠后面,那么它是否也能与水反应呢?
【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂。实验过程和现象如图:

【反思与总结】
(1)小明得出的实验结论是________________________________。
(2)小明发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了。
猜想 | 验证方案 |
可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色的溶液________,如果溶液变红,说明小明的猜想正确 |
小明通过实验证明了自己的猜想是正确的。
(3)一段时间后,小明观察到镁条在热水中无现象,但当他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是________________________________________________________________________。