题目内容
【题目】物质王国的“小朋友”们手拉手围成一圈做游戏。甲为酸,丁为碱,戊为酸碱指示剂,甲、乙、丙、丁为不同类别的物质(按物质组成分类)。(游戏规则:只要相邻的物质能反应,游戏就能进行下去。)
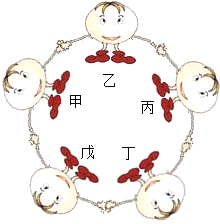
(1)写出能代表甲与丁反应的一个化学方程式_________________,其基本反应类型是____________。
(2)根据游戏规则,乙可以是___________(填物质类别),写出能代表乙与丙反应的一个化学方程式__________________________。
【答案】![]() 复分解反应 金属
复分解反应 金属 ![]()
【解析】
(1)甲为酸,丁为碱,甲与丁表示的反应是酸和碱反应生成盐和水,如:氢氧化钠和盐酸生成氯化钠和水,化学方程式![]() ,其基本反应类型是由两种化合物相互交换成分生成两种新的化合物的复分解反应;
,其基本反应类型是由两种化合物相互交换成分生成两种新的化合物的复分解反应;
(2)由于甲为酸,丁为碱,戊为酸碱指示剂,甲能够与乙反应,所以乙可以是金属(如铁),金属乙可以与盐溶液反应,某些盐溶液可以与碱反应,丙可以是盐溶液,如硫酸铜(合理即可),因铁和硫酸铜反应生成硫酸亚铁和铜,反应的方程式为:Fe+CuSO4=FeSO4+Cu;氢氧化钠(或其他可溶性碱)与硫酸铜反应生成氢氧化铜沉淀。

 千里马走向假期期末仿真试卷寒假系列答案
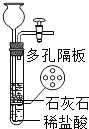
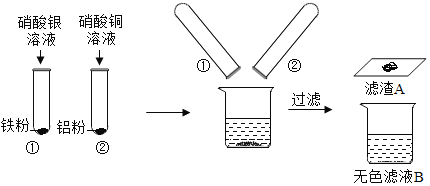
千里马走向假期期末仿真试卷寒假系列答案【题目】某班同学为验证碳酸钠的化学性质,向盛有碳酸钠的试管中加入一定量的稀盐酸,迅速用带导管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中(如图所示)。请回答问题:
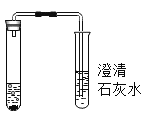
(1)右侧试管中澄清石灰水变浑浊的化学反应方程式为________。
(2)实验结束后,将两支试管中的所有物质倒入同一个废液缸中,充分反应后得到澄清溶液。同学们对废液中溶质的成分进行如下探究(忽略二氧化碳的影响) :
[提出问题]
废液中溶质的成分是什么?
[做出猜想]
猜想一: CaCl2、NaCl和HCl
猜想二: CaCl2、NaCl和Na2CO3
猜想三:______;
[进行讨论]
经过讨论,同学们一致认为猜想________是错误的。
[设计实验]
甲同学取少量废液于试管中,向其中加入硝酸银溶液,观察到白色沉淀,甲同学得出实验结论:猜想一正确。请你评价甲同学的实验及结论________。
请帮助乙同学完成实验报告
实验步骤 | 实验现象 | 实验结论 |
取少量废液于试管中,加入_________溶液 | 溶液中先产生气泡,后产生白色沉淀 | 猜想一成立 |
[反思拓展]
最终同学们确认了废液中溶质的成分。若将废液直接排入铸铁管道,危害是_______,可以加入过量的______(写化学式)处理废液,使之达到中性后排放。
【题目】氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙![]() 遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的
遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的![]() 加入
加入![]() 溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
(提出问题)滤液中溶质的成分是什么?
猜想一:NaOH猜想二:NaOH、![]()
猜想三:NaOH、![]() 猜想四:NaOH、
猜想四:NaOH、![]() 、
、![]()
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因______。
(实验验证)
实验 | 现象 | 结论 |
| 无明显现象 | 猜想 ______ 不成立 |
| ______ | 猜想三成立 |
(反思与拓展)
![]() 写出氢化钙
写出氢化钙![]() 与水反应的化学方程式______。
与水反应的化学方程式______。
![]() 若向
若向![]() 的溶液中加入一定量的
的溶液中加入一定量的![]() ,充分反应,产生的气体有氢气和______。
,充分反应,产生的气体有氢气和______。
![]() 登山运动员携带
登山运动员携带![]() 作为能源提供剂与携带氢气相比,其优点是______
作为能源提供剂与携带氢气相比,其优点是______![]() 写一条即可
写一条即可![]() 。
。