题目内容
将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有明显现象.据此判断,三种金属的金属活动性顺序是
A.甲>铜>乙 B.乙>铜>甲 C.铜>甲>乙 D.甲>乙>铜.
A
A
.A.甲>铜>乙 B.乙>铜>甲 C.铜>甲>乙 D.甲>乙>铜.
分析:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此根据能否发生反应,可确定三种金属活动性由强到弱的顺序.
解答:解:将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,说明甲的金属活动性比铜强,即甲>铜;乙没有明显现象,说明乙的金属活动性比铜弱,即Cu>乙.则三种金属的金属活动性顺序是甲>铜>乙.
故答案为:A.
故答案为:A.
点评:本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.

练习册系列答案
相关题目


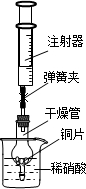
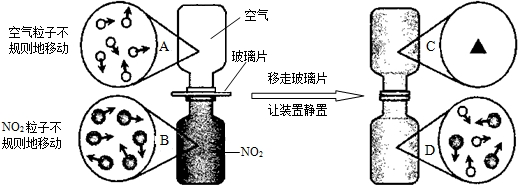
 (京京同学对金属活动性顺序等知识进行了研究.
(京京同学对金属活动性顺序等知识进行了研究.