题目内容
【题目】现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是

A.生成氢气的质量:甲>乙>丙.
B.相对原子质量:丙>乙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:丙>乙>甲
【答案】D
【解析】
如图所示等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,金属活泼性越强,金属与质量分数相同的稀硫酸反应速率越快,已知产生氢气的速率为乙>甲>丙,则金属的活泼性为乙>甲>丙;已知甲、乙、丙在生成物中化合价均为+2价,金属的相对原子质量越小,等质量的金属,与溶质质量分数相同的足量稀硫酸反应产生氢气越多,图中生成氢气的质量甲>乙>丙,则三种金属元素原子相对原子质量的大小关系为丙>乙>甲。
A、由图可知生成氢气的质量:甲>乙>丙,A选项说法正确,不符合题意;
B、由以上分析可知相对原子质量:丙>乙>甲,B选项说法正确,不符合题意;
C、由以上分析可知金属活动性:乙>甲>丙,C选项说法正确,不符合题意;
D、由题意生成氢气越多,消耗稀硫酸越多,则消耗硫酸的质量:甲>乙>丙,D选项说法不正确,符合题意。故选D。

【题目】操作和保存药品不当,标签常常易损毁。现有四瓶溶液①②③④的试剂标签已破损(如下图),但是已经知道这四瓶试剂是NaOH、Ca(OH)2、Na2CO3、KCl 溶液中的一种,某兴趣小组的同学决定对四瓶破损标签溶液成分进行实验探究(实验中另外的药品提供盐酸和酚酞溶液):
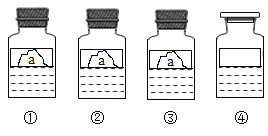
[提出问题]标签已经破损的①②③④四瓶溶液分别是什么溶液?
[实验探究1]第④瓶试剂肯定是_____(写化学式)。
[实验探究2]兴趣小组对①②③瓶溶液进行了如下的实验探究:
序号 | 实验步骤 | 实验现象 | 实验结论 |
1 | 取①②③瓶溶液少量于三支试管中,分别加入酚酞溶液 | _____ | 酚酞溶液不能将这三种溶液鉴别出来 |
2 | 再取①②③瓶溶液少量于另外三支试管中,分别加入_____溶液 | 盛有①溶液的试管中_____;其余两支试管中无明显现象 | ①瓶溶液为Na2CO3 |
3 | 取②③瓶溶液少量于两支试管中,分别加入_____溶液 | 盛有②溶液的试管中:_____;盛有③溶液的试管中:_____ | ②瓶溶液为_____ ③瓶溶液为Ca(OH)2 |