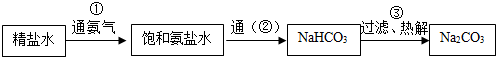
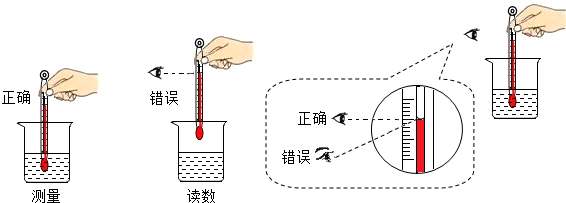
题目内容
如图甲是浓硫酸试剂瓶标签的部分内容:

(1)用该浓硫酸配制200g 19.6%的稀硫酸,需要这种浓硫酸的质量为 g.
(2)向20g某氢氧化钠溶液中,逐滴加入19.6%的稀硫酸,加入稀硫酸的质量[mH2SO4]和混合溶液的PH的变化 关系如图乙所示,计算该氢氧化钠溶液中溶质的质量分数.

(1)用该浓硫酸配制200g 19.6%的稀硫酸,需要这种浓硫酸的质量为
(2)向20g某氢氧化钠溶液中,逐滴加入19.6%的稀硫酸,加入稀硫酸的质量[mH2SO4]和混合溶液的PH的变化 关系如图乙所示,计算该氢氧化钠溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:溶液稀释前后,溶质质量不变;
根据稀硫酸的质量、质量分数可以计算氢氧化钠的质量,进一步可以计算氢氧化钠溶液的质量分数.
根据稀硫酸的质量、质量分数可以计算氢氧化钠的质量,进一步可以计算氢氧化钠溶液的质量分数.
解答:解:(1)设需要浓硫酸的质量为x,
x×98%=200g×19.6%,
x=40g,
故填:40;
(2)由图中信息可知,当加入20g稀硫酸时,溶液的pH=7,说明氢氧化钠和稀硫酸恰好完全反应,设氢氧化钠的质量为y,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
y 20g×19.6%
=
,
y=3.2g,
该氢氧化钠溶液中溶质的质量分数为:
×100%=16%,
答:该氢氧化钠溶液中溶质的质量分数为16%.
x×98%=200g×19.6%,
x=40g,
故填:40;
(2)由图中信息可知,当加入20g稀硫酸时,溶液的pH=7,说明氢氧化钠和稀硫酸恰好完全反应,设氢氧化钠的质量为y,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
y 20g×19.6%
| 80 |
| y |
| 98 |
| 20g×19.6% |
y=3.2g,
该氢氧化钠溶液中溶质的质量分数为:
| 3.2g |
| 20g |
答:该氢氧化钠溶液中溶质的质量分数为16%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列溶液露置在空气中,由于发生化学变化而使溶质质量增大的是( )
| A、浓硫酸 | B、氢氧化钠溶液 |
| C、浓盐酸 | D、氯化钠溶液 |
学习化学的目的,不在于要成为化学家,重要的是要善于运用化学知识去分析、解决生产、生活中的问题.从化学角度看,下列说法中错误的是( )
| A、进入久未开启的地窖时要先做灯火实验 |
| B、用食醋浸泡可除去热水瓶内的水垢 |
| C、将表面生锈的铁制品长时间浸没在过量的稀盐酸中,以除去铁锈 |
| D、在蚊叮虫咬的皮肤处涂抹肥皂水或牙膏以减少疼痛 |
除去氯化钠中的少量碳酸钠,下列方法不能实现的是( )
| A、加适量盐酸,蒸发结晶 |
| B、加适量Ca(OH)2溶液,过滤后蒸发结晶 |
| C、加适量BaCl2溶液,过滤后蒸发结晶 |
| D、加适量CaCl2溶液,过滤后蒸发结晶 |