题目内容
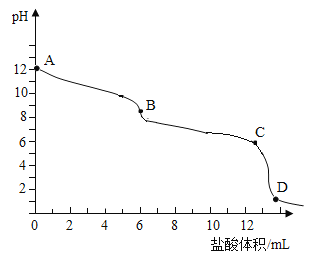
【题目】向碳酸钠溶液中滴加稀盐酸,所得溶液的 pH与消耗稀盐酸体积的变化关系如图所示已知该反应过程分为2个阶段:①Na2CO3+HCl=NaHCO3+NaCl;②NaHCO3+HCl=NaCl+H2O+CO2↑,AB段主要进行①反应,BC段主要进行②反应,下列说法正确的是( )
A.加入稀盐酸后立即产生气泡
B.碳酸氢钠溶液比碳酸钠溶液碱性弱
C.D点反应基本结束
D.D点溶液中的溶质为 NaCl
【答案】B
【解析】
A、AB段主要进行①反应,故加入盐酸不能立即产生气泡,故A错误;
B、根据图可以看出,随着反应的进行,pH不断减小,可知碳酸氢钠溶液比碳酸钠溶液碱性弱,故B正确;
C、C点时溶液的pH等于7,此时反应基本结束,达到D点溶液的pH小于7,说明盐酸已经过量,故C错误;
D、D点溶液中的溶质有NaCl,还有过量的HCl,故D错误。
故选B。

练习册系列答案
相关题目
【题目】实验室常用加热氯酸钾和二氧化锰固体混合物制取氧气。取30克氯酸钾和二氧化锰的混合物加热,测得剩余固体的质量(m)与反应时间(t)的关系如下表:
反应时间t∕s | t0 | t1 | t2 | t3 | t4 |
反应后固体的质量m∕g | 30 | 27.5 | 24.7 | 20.4 | 20.4 |
请根据相关信息完成下列计算:
(1)完全反应后,生成氧气的质量为____克?
(2)完全反应后,剩余固体中各物质的质量分别为________克?
(3)原固体混合物中氯酸钾的质量分数____?