题目内容
【题目】实验室常用加热氯酸钾和二氧化锰固体混合物制取氧气。取30克氯酸钾和二氧化锰的混合物加热,测得剩余固体的质量(m)与反应时间(t)的关系如下表:
反应时间t∕s | t0 | t1 | t2 | t3 | t4 |
反应后固体的质量m∕g | 30 | 27.5 | 24.7 | 20.4 | 20.4 |
请根据相关信息完成下列计算:
(1)完全反应后,生成氧气的质量为____克?
(2)完全反应后,剩余固体中各物质的质量分别为________克?
(3)原固体混合物中氯酸钾的质量分数____?
【答案】(1)9.6;(2)5.5g、14.9g;(3)81.7%
【解析】
(1)根据表中的数据可知t3和t4所剩固体相等,所以当时间在t4时氯酸钾已经完全反应;因此生成氧气的质量是30g-20.4g=9.6g;
(2)解:氯酸钾受热分解后剩余的固体有反应生成的氯化钾以及催化剂二氧化锰;
设反应后生成的氯化钾质量为x
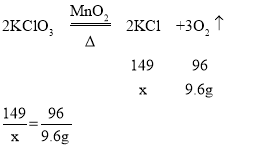
x=14.9g
剩余固体中MnO2的质量20.4g-14.9g=5.5g;
答:剩余固体中有MnO2和KCl,质量分别为:5.5g、14.9g。
(3)原固体混合物中氯酸钾的质量分数为![]() ×100%≈81.7%
×100%≈81.7%
答:原固体混合物中氯酸钾的质量分数为81.7%。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目