题目内容
【题目】如图为硝酸钾和氯化钠的溶解度曲线。回答下列问题:
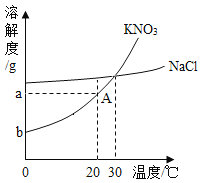
(1)当温度为30℃时,硝酸钾的溶解度_____(填“>”、“<”或“=”)氯化钠的溶解度。
(2)将A点对应KNO3溶液从20℃升温到30℃(忽略水的蒸发),在此过程中,硝酸钾的溶质质量分数_____(选填“增大”、“减小”或“不变”)。
(3)将A点对应的100gKNO3溶液恒温蒸发10g水,可析出KNO3的质量为_____g。
【答案】> 不变 0.1a
【解析】
(1)由溶解度曲线可知:当温度为30℃时,硝酸钾的溶解度大于氯化钠的溶解度;故填:>。
(2)将A对应KNO3溶液从20℃升温到30℃(忽略水的蒸发),在此过程中,硝酸钾的溶质质量分数不变,因为升温后硝酸钾溶液的溶质和溶剂都不变;故填:不变;
(3)20℃时,硝酸钾的溶解度是ag,A点时对应的硝酸钾溶液是饱和溶液,即100g水中能够溶解ag硝酸钾,则10g水中能够溶解0.1ag硝酸钾,恒温蒸发10g水时,可析出KNO3的质量为0.1ag。
故填:0.1a。

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案【题目】将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X。测得反应前后物质的质量如下表:
物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
下列判断正确的是
A.表中m的值为13.5B.该反应属于分解反应
C.物质X能在氧气中燃烧D.物质X中一定含有氢元素
【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。下列关于此反应的认识,正确的是
物 质 | X | Y | Z | W |
反应前的质量(g) | 20 | m | 16 | 14 |
反应后的质量(g) | 4 | 6 | 60 | 50 |
A.m的数值为64
B.若W为水,则X或Y必定为酸或碱
C.参加反应的X与Y的质量比为1︰4
D.若X为化合物,Y为单质,则该反应一定为置换反应