题目内容
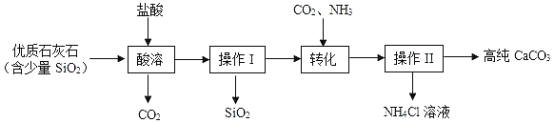
【题目】高纯碳酸钙广泛应用于电子、医药等领域。某化工厂利用优质石灰石(含少量SiO2等不溶于水和稀盐酸的杂质)为原料得到高纯CaCO3.其工艺流程如图。
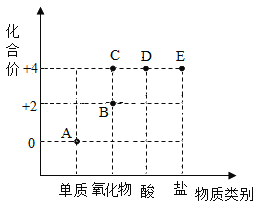
(1)SiO2中Si的化合价:____________。
(2)实验室进行操作I的名称是_____________。
(3)请完成“转化步骤中发生反应的化学方程式:________。
(4)该工艺的副产品NH4Cl的用途有__________(写出一种即可)。
【答案】+4价 过滤 CaCl2+CO2+2NH3+H2O=2NH4Cl+CaCO3↓ 作氮肥
【解析】
(1)根据化合价代数和为零,设硅元素化合价为x,则x+(-2)×2=0,x=+4,故填:+4价。
(2)固液分离的操作是过滤,故填:过滤。
(3)碳酸钙和盐酸反应生成氯化钙二氧化碳和水,操作I之后得到氯化钙溶液,通入二氧化碳和氨气生成氯化铵和碳酸钙,化学方程式为CaCl2+CO2+2NH3+H2O=2NH4Cl+CaCO3↓,故填:CaCl2+CO2+2NH3+H2O=2NH4Cl+CaCO3↓。
(4)氯化铵含氮元素可作氮肥,故填:作氮肥。

【题目】某化学兴趣小组同学为确定无色溶液X中的溶质,含碳酸钠、碳酸氢钠、氢氧化钠中的至少两种,开展了探究活动,请你一同参与。
(查阅资料)(1)CaCl2﹑NaCl溶液都呈中性,与NaHCO3溶液都不会反应
(2)NaHCO3溶液呈碱性,![]()
(3)NaOH与Ca(OH)2有相似的化学性质
(猜想与假设)猜想一:溶液X含有NaOH﹑Na2CO3
猜想二:溶液X含有Na2CO3﹑NaHCO3
猜想三:溶液X含有NaOH﹑NaHCO3﹑Na2CO3
针对猜想,有同学提出猜想三是错误的,其理由_______(用化学方程表示)。
(实验方案设计)
序号 | 实验步骤 | 预设实验现象 | 预设实验结论 |
① | 取样于烧杯中,滴入过量的氯化钙溶液,过滤, | _____ | 猜想一成立。 |
② | 取①的滤液于试管中,滴入适量的氢氧化钙溶液, | 无明显现象, | 猜想二__。 |
③ | 取①的滤液于试管中,滴入___溶液, | 溶液变红色 | 猜想_成立。 |
(结论与反思)由实验,得无色溶液X的溶质是NaOH﹑Na2CO3,经讨论后,有同学提出实验①的结论不完善,其理由是_____。