题目内容
【题目】某小组同学利用下图所示装置探究了可燃物的燃烧条件。已知:白磷的着火点40℃,棉花的着火点150℃。
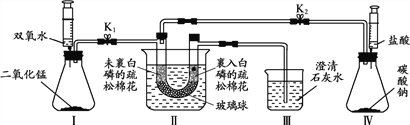
步骤①:将U型管放入冷水中,打开K1,关闭K2,向U型管中充入氧气。两端棉花都不燃烧。
步骤②:打开K2,关闭K1,向U型管中充入二氧化碳,观察到澄清石灰水变浑浊后,将U型管放入80℃热水中。两端棉花都不燃烧。
步骤③:······
步骤④:打开K2,关闭K1,向U型管中充入二氧化碳。燃烧着的棉花熄灭。
(1)步骤①的实验目的是_________________。
(2)步骤②中澄清石灰水的作用是_________________。
(3)步骤③的操作及现象是_________________。
(4)步骤④中燃着的棉花熄灭的原因是_________________。
【答案】 探究可燃物与氧气接触,温度未达到着火点时是否燃烧 证明U型管中氧气已排尽 打开K1,关闭K2,向U型管中充入氧气。右端棉花燃烧,左端棉花不燃烧 充入不支持燃烧的二氧化碳,隔绝了氧气
【解析】(1)步骤①:将U型管放入冷水中,打开K1,关闭K2,向U型管中充入氧气,两端棉花都不燃烧,试验目的是:探究可燃物与氧气接触,温度未达到着火点时是否燃烧;(2) 打开K2,关闭K1,向U型管中充入二氧化碳,观察到澄清石灰水变浑浊后,证明U型管中氧气已排尽;(3)分析整个实验,步骤③的目的是探究燃烧是否与氧气有关,所以步骤③的操作及现象是:打开K1,关闭K2,向U型管中充入氧气。右端棉花燃烧,左端棉花不燃烧;(4)步骤④中燃着的棉花熄灭的原因是:向U型管中充入二氧化碳后隔绝了氧气。

【题目】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取80g石灰石样品等分为4份(分别编号为①、②、③、④),每份样品分别与一定量的稀盐酸反应,所得数据如表所示:
样品编号 | ① | ② | ③ | ④ |
稀盐酸的质量 | 50g | 100g | m(150<m<250) | 250g |
剩余固体的质量 | 15g | 10g | 4g | 4g |
然后,为了探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将编号③所得溶液过滤,取滤液质量的1/8于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
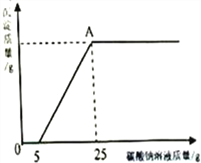
分析题中有关信息和图表(横坐标表示碳酸钠溶液、纵坐标为生成沉淀质量),回答下列问题:
(1)该石灰石样品的纯度为______.所用盐酸的溶质质量分数为__________。
(2)编号③所用稀盐酸的质量m为______g.
(3)A点处对应的溶液中溶质的质量是________?(写出计算过程)