题目内容
回答下列问题:
(1)请用化学用语表示: 3个钾原子 ,2个氮分子 ;
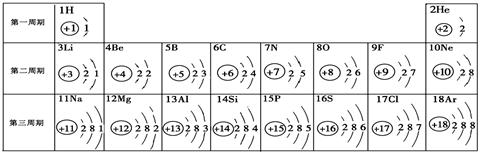
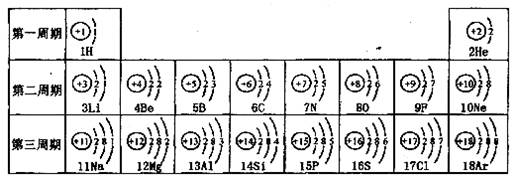
(2)右图是铝的结构示意图和在周期表中的位置图,则铝原子的核电荷数是 ,铝元素的相对原子质量是 ;

(3)K2Cr2O7(重铬酸钾)和KMnO4是重要的化学试剂。
①K2Cr2O7中铬元素的化合价是 ,硫酸铬(铬元素为+3价)的化学式为 。
②KMnO4是紫黑色的固体,它可用于制取氯气,发生反应的化学方程式为:
2KMnO4 + 16HCl =" 2KCl" + 2X + 5Cl2↑+ 8H2O,请写出X物质的化学式 。
(1)请用化学用语表示: 3个钾原子 ,2个氮分子 ;
(2)右图是铝的结构示意图和在周期表中的位置图,则铝原子的核电荷数是 ,铝元素的相对原子质量是 ;

(3)K2Cr2O7(重铬酸钾)和KMnO4是重要的化学试剂。
①K2Cr2O7中铬元素的化合价是 ,硫酸铬(铬元素为+3价)的化学式为 。
②KMnO4是紫黑色的固体,它可用于制取氯气,发生反应的化学方程式为:
2KMnO4 + 16HCl =" 2KCl" + 2X + 5Cl2↑+ 8H2O,请写出X物质的化学式 。
(1)3K 2N2 (2)13 26.98 (3)+6 Cr2(SO4)3
(4) MnCl2
(4) MnCl2
试题分析:(1)根据化学符号及其周围数字的意义分析解答。
标在元素符号前面的数字表示原子的个数,故3个钾原子表示为3K;
标在化学式前面的数字表示分子的个数,故2个氮气分子表示为2N2。
(2)根据元素周期表中的一个小格提供的信息可知,元素符号前面的数字为原子序数,故铝元素的原子序数为13,而原子序数=核电荷数,故其核电荷数为13;元素名称的下方数字为该元素的相对原子质量,故铝元素的相对原子质量为26.98。
(3)①根据化合价的原则,“在化合物中,正负化合价的代数和为零”,已知K的化合价为+1价,O的化合价为-2价,设K2Cr2O7中Cr元素的化合价为x,则(+1)×2+2x+(-2)×7=0,解得x=+6价;已知硫酸根的化合价为-2价,铬元素为+3价,根据化学式的书写方法,正价在左,负价在右,正负化合价的代数和为零,可知硫酸铬的化学式为Cr2(SO4)3。
②由反应的化学方程式2KMnO4 + 16HCl =" 2KCl" + 2X + 5Cl2↑+ 8H2O可知,
反应前 反应后
K原子 2 2
Mn原子 2 0
O原子 8 8
H原子 16 16
Cl原子 16 12
根据质量守恒定律,化学变化前后原子的种类、数目不变,可判断生成物2X分子中含有2个Mn原子和4个Cl原子,则1个X分子中含有1个Mn原子和2个Cl原子,则物质X的化学式为MnCl2。
点评:本题难度不大,但考查的知识点较多,且多为对基础知识的考查,所以同学们在日常的学习中要注意相关知识的积累。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 W+3H2O的反应中,还原剂是( )
W+3H2O的反应中,还原剂是( )
 SO2
SO2 2CO
2CO