题目内容
【题目】阅读下列科普材料,回答相关问题。
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物。其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业。葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动。食糖加工过程中可使用SO2进行脱色。按照我国《食品添加剂使用标准(GB2760-2014)》,合理使用SO2不会对人体健康造成危害。
标准中部分食品的SO2最大残留量
食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大残留量 | 0.35 g/kg | 0.25 g/L | 0.1 g/kg | 0.1 g/kg | 0.1 g/kg | 0.05 g/kg |
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化。工业利用硫制硫酸的主要过程示意如下:
![]()
硫酸工业尾气中含有少量的SO2,若直接排放会污染空气,并导致硫酸型酸雨。工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用。
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2。为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量、改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量。
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题。
(1)按照国家标准,食糖中的SO2最大残留量为______ g/kg;
(2)用硫制硫酸的主要过程中,涉及到的含硫物质有S、______和H2SO4;
(3)硫酸工业生产中,吸收尾气中SO2的物质是______;
(4)下列措施能减少SO2排放的是______(填序号);
A 将煤块粉碎 B 对燃煤进行脱硫
C 推广煤改气、煤改电 D 循环利用工业尾气中的SO2
(5)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下所示:![]() ,这种脱硫技术称为微生物脱硫技术。写出该技术中的第二步化学反应方程式:______。
,这种脱硫技术称为微生物脱硫技术。写出该技术中的第二步化学反应方程式:______。
【答案】0.1 SO2、SO3 氨水 BCD 4FeSO4+2H2SO4+O2 ![]() 2Fe2SO4+2H2O
2Fe2SO4+2H2O
【解析】
(1)由图可知,食糖中的SO2最大残留量为0.1g/kg,故填0.1。
(2)由工业利用硫制硫酸的主要过程示意如下:![]() 可知,用硫制硫酸的主要过程中,涉及到的含硫物质有S、SO2、SO3和H2SO4,故填SO2、SO3。
可知,用硫制硫酸的主要过程中,涉及到的含硫物质有S、SO2、SO3和H2SO4,故填SO2、SO3。
(3)由题文可知,硫酸工业生产中,吸收尾气中SO2的物质是氨水,故填氨水。
(4)A 将煤块粉碎并不能改变煤中的含硫量,最终生成的二氧化硫的质量不变,选项错误;
B 对燃煤进行脱硫可以降低生成二氧化硫的质量,选项正确;
C 推广煤改气、煤改电可以降低二氧化硫的排放量,从而改善空气质量,选项正确;
D 循环利用工业尾气中的SO2,可以减少二氧化硫的排放,选项正确,故填BCD。
(5)该反应是硫酸亚铁、硫酸和氧气在微生物作用下反应生成硫酸铁和水,故反应的化学方程式写为:4FeSO4+2H2SO4+O2 ![]() 2Fe2SO4+2H2O 。
2Fe2SO4+2H2O 。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
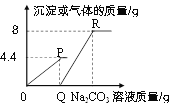
同步拓展阅读系列答案【题目】某氢氧化钙样品中含碳酸钙杂质,现称取研细的该样品12.4g放入锥形瓶中,加入32.6g的水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生。测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表示:
加入盐酸的质量g | 0 | 25 | 37.5 |
锥形瓶中物质的质量g | 45 | 70 | 80.3 |
请你完成以下问题:
(1)加入盐酸的质量在0—25g时,______与盐酸发生反应;
(2)求样品中氢氧化钙的质量分数(写出计算过程,精确到0.1%)。______。