题目内容
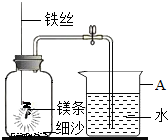 某校研究性学习小组用镁条代替红磷验证空气中氧气含量测定的实验,最后发现进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用镁条代替红磷验证空气中氧气含量测定的实验,最后发现进入集气瓶中水的体积约占集气瓶容积的70%.【发现问题】如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
21
21
%.【提出假设】进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体,其中氮元素的化合价是
-3
-3
价.【实验验证】兴趣小组到医院中购买了一袋的氮气并收集到集气瓶中,将镁条点燃后伸入瓶中,发现镁条果然能继续燃烧着,该反应的方程式式为
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
,该反应属于
| ||
化合反应
化合反应
(填化合或分解)反应.【拓展应用】通过以上探究,兴趣小组同学明白了探究空气中氧气含量的实验中不能用镁条代替红磷,同时也对物质的燃烧有了什么新的认识:如
燃烧不一定有氧气参加
燃烧不一定有氧气参加
(写出一点即可).分析:【发现问题】根据空气中氧气的体积为21%以及氮气不溶于水进行解答;
【查阅资料】根据化合物中各元素的化合价代数和为0以及镁元素的化合价为+2价进行解答;
【实验验证】根据镁条和氮气反应生成氮化镁进行解答;
【拓展应用】根据燃烧不一定有氧气参加进行解答.
【查阅资料】根据化合物中各元素的化合价代数和为0以及镁元素的化合价为+2价进行解答;
【实验验证】根据镁条和氮气反应生成氮化镁进行解答;
【拓展应用】根据燃烧不一定有氧气参加进行解答.
解答:解:【发现问题】空气中氧气的体积为21%,氮气不溶于水,所以如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%;
【查阅资料】由化合物中各元素的化合价代数和为0以及镁元素的化合价为+2价,所以氮化镁(Mg3N2)中氮元素的化合价是-3价;
【实验验证】镁条和氮气反应生成氮化镁,反应的方程式式为3Mg+N2
Mg3N2;由两种物质反应生成一种物质属于化合反应;
【拓展应用】根据镁条在氮气中能燃烧,可知燃烧不一定有氧气参加.
故答案为:【发现问题】21;
【查阅资料】-3;
【实验验证】3Mg+N2
Mg3N2;化合反应;
【拓展应用】燃烧不一定有氧气参加
【查阅资料】由化合物中各元素的化合价代数和为0以及镁元素的化合价为+2价,所以氮化镁(Mg3N2)中氮元素的化合价是-3价;
【实验验证】镁条和氮气反应生成氮化镁,反应的方程式式为3Mg+N2
| ||
【拓展应用】根据镁条在氮气中能燃烧,可知燃烧不一定有氧气参加.
故答案为:【发现问题】21;
【查阅资料】-3;
【实验验证】3Mg+N2
| ||
【拓展应用】燃烧不一定有氧气参加
点评:根据对空气组成成分的认识,利用镁的性质及题中资料信息,分析导致实验中所出现现象的可能性,考查获得信息解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
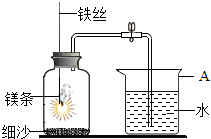 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.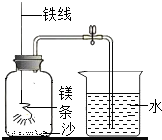 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.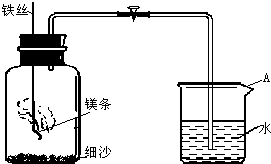
 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹.