题目内容
【题目】近几年餐饮行业经常使用一种“固体酒精”,替代相对不够安全的液体酒精,化学兴趣小组的同学对“固体酒精”产生了好奇,并对其成分进行研究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
(2)氯化钙、氯化钡溶液均呈中性。
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
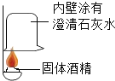
【实验探究】(1)按下图实验,发现澄清石灰水变浑浊,证明生成了CO2,可得出酒精中含有碳元素的结论。写出澄清石灰水变浑浊的化学方程式:
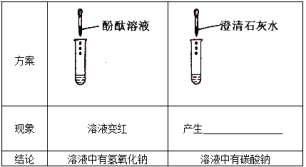
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀。取沉淀于试管中加稀盐酸,有气泡产生。分析实验并结合资料得出氢氧化钠已变质。①写出氢氧化钠变质的化学方程式:
②据上述信息写出产生沉淀的化学方程式:
(3)为进一步确定氢氧化钠的变质程度,分组探究。
①甲组取烧杯上层清夜于两支试管中,按右图探究。
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是 。他们另取烧杯中上层清夜,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红。
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质。
【反思交流】乙组实验中加足量氯化钡溶液的目的是
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的 。
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
【答案】(1)CO2 +Ca(OH)2 = CaCO3↓+ H20 白色沉淀(表格中答案)
(2)CO2+2NaOH = Na2CO3 + H2O、Na2CO3+ CaCl2 = CaCO3↓+2NaCl
(3)Na2CO3溶液呈碱性,也能使酚酞溶液变红。除去Na2CO3(或CO32-),防止干扰NaOH的检验。
【拓展应用】AC
【解析】
试题分析:【实验探究】澄清石灰水变浑浊是因为石灰水与CO2反应即CO2 +Ca(OH)2 = CaCO3↓+ H20;
氢氧化钠变质是氢氧化钠与空气中的CO2作用的结果即CO2+2NaOH = Na2CO3 + H2O;产生沉淀为Na2CO3+ CaCl2 = CaCO3↓+2NaCl;
(3)因为NaOH变质生成的碳酸钠呈碱性,也能使酚酞溶液变红;
【反思交流】加足量氯化钡溶液,除去Na2CO3(或CO32-),防止干扰NaOH的检验。
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的氢氧化钡溶液、氢氧化钙溶液,不能选择氯化钙溶液,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此使用氯化钙时能够带入新杂质--氯化钠.

【题目】实验室利用下图实验装置进行有关化学实验,请回答下列问题:

(1)写出图中指定仪器的名称:① ;② 。
(2)实验室用氯酸钾和二氧化锰制取氧气,发生装置可选择图中的 (填字母),该反应的化学方程式为: 。
(3)某同学想通过装置C收集二氧化碳,气体应从 (填“a”或“b”)进入。
(4)对上述制取二氧化碳实验后的固液残留物进行分离,可选择上图中的装置 (填字母),该操作中玻璃棒的作用是 。
(5)某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 充分反应后 | ||
实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
180 g | 12g | 187.6g | |
求该石灰石中碳酸钙的质量分数。(计算结果保留一位小数)

