题目内容
【题目】(发现问题)研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
(实验探究)在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如图所示,请你一起参与。
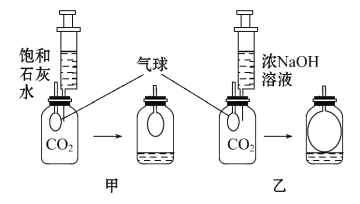
(现象结论)甲装置中产生的实验现象_________(用化学方程式表示),解释通常用石灰水而不用浓NaOH溶液检验CO2的原因_________;乙装置中的实验现象是_____________;
(计算验证)另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH。因此,他认为通常吸收CO2应该用饱和石灰水。
(思考评价)请你对小李同学的结论进行评价:_________。
【答案】CO2+Ca(OH)2CaCO3↓+H2O CO2与石灰水作用有明显实验现象,与NaOH作用无明显现象 气球体积增大,溶液不变浑浊 不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中溶质的质量分数很小
【解析】
根据二氧化碳能和石灰水反应生成碳酸钙沉淀和水,氢氧化钠能和二氧化碳反应生成易溶于水的碳酸钠和水,氢氧化钙在水中的溶解度小,氢氧化钠在水中的溶解度大进行分析。
[现象结论] 二氧化碳与澄清的石灰水反应生成碳酸钙沉淀,通过这一现象,可以用澄清的石灰水来检验二氧化碳的存在,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;通常用石灰水而不用浓NaOH溶液检验CO2的原因是:CO2与石灰水作用有明显实验现象,与NaOH作用无明显现象;由图可知,乙装置中的实验现象是:气球体积增大,溶液不变浑浊;
[思考评价] 小李同学的结论不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中溶质的质量分数很小。

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案