籾朕坪否
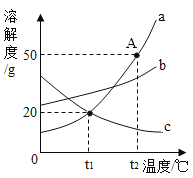
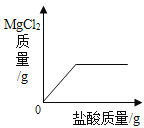
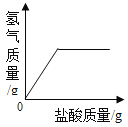
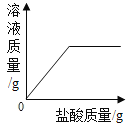
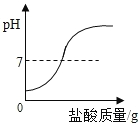
‐籾朕/蝶墳嗟晒垢皆晒刮片議糞刮埀喘15%議狽剳晒墜卑匣牢脚匯協楚墳嗟恢瞳嶄議火噫葬磨⇧霞誼糞刮方象泌和燕侭幣。
糞刮會催 | 嶧債NaOH卑匣議嵎楚 | 牢脚朔卑匣議pH |
〙 | 30g | pH〽7 |
〖 | 40g | pH﹆7 |
〗 | 50g | pH﹅7 |
飛匯協楚墳嗟恢瞳嶄火噫葬磨議嵎楚葎100 g⇧萩柴麻乎火噫葬磨議卑嵎嵎楚蛍方(亟竃峋聾議柴麻狛殻)。__________
‐基宛/7.35%
‐盾裂/
功象狽剳晒墜才葬磨郡哘伏撹葬磨墜才邦⇧卆象如挫頼畠郡哘議方象序佩柴麻⤴宥狛蛍裂燕嶄議方象辛岑⇧糞刮〖郡哘朔⇧卑匣議pH峙吉噐7⇧曾宀如挫頼畠郡哘⇧侭參哘乎僉夲糞刮會催〖議方象。
盾⦿譜火噫葬磨嶄卑嵎議嵎楚葎x⇧
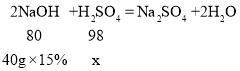
![]()
x=7.35g⇧
火噫葬磨嶄卑嵎議嵎楚蛍方=![]() 〜100%=7.35%◉
〜100%=7.35%◉
基⦿火噫葬磨嶄卑嵎議嵎楚蛍方葎7.35%。

 豚挑鹿潤催狼双基宛
豚挑鹿潤催狼双基宛‐籾朕/僥楼阻MnO2斤狛剳晒狽蛍盾嗤岸晒恬喘議岑紛朔⇧蝶揖僥峐⦿CuO嬬倦軟欺窃貌MnO2議岸晒質恬喘椿◦噐頁序佩阻參和冥梢⤴
↙佳峐⇄↔CuO音頁岸晒質、匆音歌嚥郡哘⇧郡哘念朔嵎楚才晒僥來嵎音延◉
ÅCuO歌嚥郡哘恢伏O2⇧郡哘念朔嵎楚才晒僥來嵎窟伏阻個延◉
‰CuO頁郡哘議岸晒質⇧郡哘念朔__________________⤴
↙糞刮⇄喘爺峠各楚0.2gCuO⇧函5mL5%議狛剳晒狽卑匣噐編砿嶄⇧序佩泌和糞刮⦿
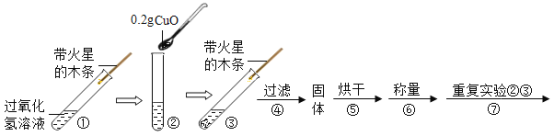
↙1⇄野亟和燕⦿
化帶〗孖嵆 | 化帶⌒潤惚 | 化帶∂孖嵆 | 潤胎 |
____________揮諮佛議直訳鹸伴⤴ | ________ | 卑匣嶄嗤賑倒慧竃⇧ ___________ | 佳峐↔、Å音撹羨◉佳峐‰撹羨⤴ |
↙2⇄化帶〙議朕議頁_____________________⤴
↙3⇄狛剳晒狽嬬瓜CuO岸晒蛍盾慧竃O2議猟忖燕器塀葎________________⇧凪嶄CuO斤郡哘伏撹議剳賑議謹富________↙野^嗤 ̄賜^涙 ̄⇄唹峒。